Novinky-vrozená leukémie po těžkém zneužívání permethrinového spreje během těhotenství

ZPRÁVA
Vrozené leukémie po těžké zneužívání permethrin sprej během těhotenství
Borkhardt, M Wilda, U. Fuchs, L Gortnerovu a já Reiss
dětské fakultní Nemocnice Giessen, Feulgenstr 12, 35392 Giessen, Německo
kontakt:
Dr Borkhardt, dětské Hematologie a Onkologie, Feulgenstr 12, 35392 Giessen, Německo;
arndt.borkhardt{at}paediat.med.uni-giessen.de
přijato 6. října 2002
abstrakt
je popsán jediný případ vrozené leukémie s přeskupením 11q23/MLL u předčasně narozeného novorozence. Kvůli arachnofobii matka silně zneužívala aerosolizovaný permethrin, široce používaný domácí insekticid. Permethrin je považován za poměrně bezpečný, ale s ohledem na historii matky byl testován jeho potenciál indukovat štěpení genu MLL v buněčné kultuře. Inkubace buněčné linie BV173 s 50 µM permethrinem snadno vyvolala štěpení MLL.
klíčová slova: kongenitální leukémie; leukémie; permethrin; insekticid; 11q23/MLL
vrozená leukémie je vzácné onemocnění, které postihuje asi jedno dítě v 200 000-250 000 živě narozených ročně. Navzdory své vzácnosti vrozená leukémie vyvolala velký zájem kvůli příležitosti dozvědět se více o základních příčinách in utero leukemogeneze. Existuje mnoho rizikových faktorů, které mohou zvýšit pravděpodobnost časné indukci a fenotyp leukemických—například rodičovská expozice na pracovišti a životního prostředí toxiny, užívání tabáku, marihuany, alkoholu a jiných toxinů.1 Vrozené a kojenecké leukémie jsou často spojeny s přestavby v MLL genu na chromozomu 11q23.2 Několik látek byly zkoumány pro jejich potenciál přes placentární bariéru a vyvolat takové chromozomální přestávka na 11q23/MLL.3,4
zde rozšiřujeme seznam léků schopných štěpit Gen MLL, alespoň když jsou buňky vystaveny v kultuře. Spolu s poměrně neobvyklou anamnézou, naše experimentální údaje vrhly světlo na generování vrozené leukémie a mohou pomoci zabránit některým smrtelným případům této nemoci.
kazuistika
27letá zdravá žena byla přijata na gynekologické oddělení kvůli předčasnému porodu. Byla v 35. týdnu svého prvního těhotenství. Prenatální kontroly byly normální. Protože kardiotokogram nevykazoval žádný fetální srdeční rytmus, byl naplánován nouzový císařský řez. Nicméně, o šest minut později, žena spontánně porodila předčasně narozené dítě váží 2300 g a ukazovat žádné známky života, ale zarážející vzteky bez sebe barvu kůže. Primární kardiopulmonální resuscitace byla zahájena okamžitě endotracheální intubací, kompresí hrudníku a opakovaným podáváním adrenalinu. Skóre Apgar však zůstalo 0 po pěti a 10 minutách. Pediatrický pohotovostní tým dorazil o 10 minut později a pokračoval v kardiopulmonální resuscitaci. Centrální linie byla dosažena katetrizací pupeční žíly. Po 25 minutách po porodu byla stanovena stabilní cirkulace se srdeční frekvencí 140 tepů / min. Fyzikální vyšetření prokázalo hepatomegalii 5 cm pod žebry a tvárné vzteky bez sebe infiltrace kůže (obr 1A níže).
|
|
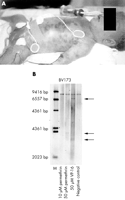
Obrázek 1 (A) pacient po 2 hodinách věku. Všimněte si leukemické infiltrace kůže („borůvkové skvrny“). B) Jižní skvrna vykazující přeskupení MLL v buněčné linii BV173 inkubované 50 µM permethrinem po dobu šesti hodin. VP16 indukované MLL štěpení bylo použito jako kontrola. |
na Rozdíl od normální anatomie srdce, ultrazvuk ukázal významné plicní hypertenze v kombinaci s druhým až třetím stupněm insuficience trikuspidální chlopně. Kromě hepatomegalie bylo zjištěno bilaterální intrakraniální krvácení. Pro dostatečné okysličení krve a odstraňování oxidu uhličitého, vysokofrekvenční ventilace bylo potřeba s 10 Hz, FIO2 = 1, a střední tlak v dýchacích cestách 13 cm H2O. Počáteční počet bílých krvinek byl 400 000/µl s přebytkem myeloidní blastické buňky. Vyšetření kostní dřeně potvrdilo diagnózu kongenitální akutní myeloidní leukémie, s 95% blast buněk myelomonocytární morfologie (FAB-M5). Byla provedena kompletní výměna krve, která snížila počet bílých krvinek na 56 000 / µl a vedla ke zlepšení okysličení a ventilace. O dvanáct hodin později se počet bílých krvinek opět zvýšil na 125 000 / µl. Mimotělní membránová oxygenace byla zvažována, ale nakonec zamítnuta z důvodu progresivního intrakraniálního krvácení zahrnujícího velkou oblast parenchymu. Kojenec zemřel 48 hodin po porodu na multiorgánové selhání. Kromě závažného poškození mozku, které již bylo diagnostikováno ultrazvukem, pitva ukázala difúzní infiltraci plic, jater, sleziny a cutis.
BUNĚČNÉ KULTURY EXPERIMENTY: INDUKCE MLL PŘESTAVEB TÍM PERMETHRIN
experimentální test byl proveden přesně tak, jak popsal Strick et al,3 kteří analyzovali širokou škálu přírodních látek v potravinách a potravinových doplňků pro jejich schopnost vyvolat konkrétní místo štěpení v rámci MLL genu.
VÝSLEDKY A DISKUSE
Cytogenetická analýza aspirátu kostní dřeně ukázala přítomnost translokace t(11;19)(q23;p13) ve všech metafází. Dále jsme ukázali přeskupení onkogenu MLL na chromozomu 11q23 jižním blotováním. Rutinní imunofenotypizace prokázala expresi CD15, CD33, CD 65s a MPO (údaje nejsou zobrazeny). V předchozích studiích monoklonální protilátka 7.1 ukázal jako cenný immunophenotypic nástroj pro detekci leukemických buněk, s NG2 expresi antigenu koreluje silně s MLL přestaveb u kojenců.5,6 v našem případě však barvení touto monoklonální protilátkou zůstalo negativní, což nám bránilo v provádění dalších experimentů třídění buněk.
matka zřejmě trpěla arachnofobií od raného dětství. Dva roky před těhotenstvím začala nadužívat aerosolizovaný permethrin. Od té doby žila sama. Lidé se jí vyhýbali kvůli pronikavému zápachu v jejím domě. Permethrin je široce používaný domácí insekticid poskytující ochranu před Anopheles vektorem malárie.7,8 je také znám jako účinný lék proti svrab a veš Pediculosis capitis.9,10 ve srovnání s jinými léky je považován za bezpečný a jeho topické použití se doporučuje i u novorozenců se svrabem.11 byla však spojena s tvorbou chromozomálních aberací v buňkách kostní dřeně myší a lézí DNA v lidských lymfocytech.12-14 proto jsme předpokládali, že permethrin překročil placentu těhotné ženy a ovlivnil hematopoetické prekurzorové buňky ve vyvíjejícím se plodu, což mělo za následek leukemogenezi. Proto jsme se pokusili generovat přeskupení v onkogenu MLL in vitro vystavením buněk BV173 50 µM permethrinu. Po 24 hodinách expozice vykazovaly buňky bv173 ošetřené permethrinem jasné přeskupení MLL, zatímco neošetřené buňky vykazovaly pouze gen MLL divokého typu (obr. 1B výše). Proto důrazně doporučujeme velkou opatrnost při užívání permethrinu během těhotenství. I když definitivní závěry nelze vyvodit z jednoho ojedinělý případ, naše údaje silně naznačují, že permethrin mohou mít závažné vedlejší účinky, když plodu hematopoetické kmenové buňky jsou vystaveny v děloze. Ve stejném duchu nedávná zpráva z nadnárodní spolupráce naznačila, že užívání komárcidních léků během těhotenství je významně spojeno s kojeneckou leukémií.4 je obzvláště pozoruhodné, že autoři našli tuto asociaci pouze pro přeskupené případy MLL a ne pro případy zárodečné linie MLL. To silně argumentuje proti předpojatosti výběru v jejich studii case-control a podporuje hypotézu, že expozice in utero způsobuje přeskupení MLL.
nakonec byla matka v našem případě úspěšně léčena pro arachnofobii psychoterapií. O dva roky později porodila zdravého chlapce, který neměl žádné klinické příznaky leukémie a který je stále zdravý ve věku 13 měsíců.
poděkování
odborná technická pomoc Claudie Kellerové a Stefanie Garkischové je vděčně uznána. Děkujeme Jochen Harbott, Giessen, Německo za poskytnutí cytogenetických údajů. Imunofenotypová data byla laskavě poskytnuta W-D Ludwig, Robert Rössle Cancer Center, Humboldtova univerzita, Berlín, Německo. Molekulární studie byly podporovány německou Nadací pro rakovinu (grant 10-1658-Bo2).
- Sande JE, Arceci RJ, Lampkin BC. Vrozená a novorozenecká leukémie. Semin Perinatol 1999; 23: 274-85.
- Ford AM, Ridge SA, Cabrera ME, et al. In utero přeskupení v onkogenu souvisejícím s trithoraxem u kojeneckých leukémií. Příroda 1993; 363:358–60.
- Strick R, Strissel PL, Borgers S, et al. Dietní bioflavonoidy indukují štěpení v genu MLL a mohou přispívat k dětské leukémii. Proc Natl Acad Sci USA 2000; 97: 4790-5.
- Alexander FE, Patheal SL, Biondi A, et al. Transplacentární chemická expozice a riziko kojenecké leukémie s fúzí genu MLL. Rakovina Res 2001; 61: 2542-6.
- Smith FO, Rauch C, Williams DE, et al. Lidský homolog rat NG2, chondroitin sulfát proteoglykan, není exprimován na povrchu buněk normálních krvetvorných buněk, ale je vyjádřena akutní myeloidní leukémie výbuchy z chudých-prognóza pacientů s abnormalitami chromozomu kapela 11q23. Krev 1996; 87: 1123-33.
- Behm FG, Smith FO, Raimondi SC, et al. Lidský homolog krysy chondroitin sulfát proteoglykan, NG2, detekován monoklonální protilátka 7.1, identifikuje dětství akutní lymfoblastické leukémie s t(4;11)(q21;q23) a t(11;19)(q23;p13) a MLL genu přestavby. Krev 1996; 87: 1134-9.
- Rowland M, Durrani N, Hewitt S, et al. Permethrin léčených chaddars a top-listy: vhodné technologie pro ochranu proti malárii v Afghánistánu a dalších složitých mimořádných událostí. Trans R Soc Trop Med Hyg 1999; 93: 465-72.
- Binka FN, Mensah OA, Mills a. nákladová efektivita permethrin impregnovaných nočníků při prevenci dětské úmrtnosti v okrese Kassena-Nankana v Severní Ghaně. Zdravotní Politika 1997; 41: 229-39.
- Blanshard ME, Schofield J. Scabies: praktický přístup. Prof Péče Matka Dítě 1999; 9: 15-16.
- Dodd CS. Intervence pro léčbu headlice. Cochrane Database Syst Rev 2000; CD001165.
- Quarterman MJ, Lesher JL, Jr. Novorozenecké svrab léčit s permethrin 5% krém. Pediatr Dermatol 1994; 11:264-6.
- Cantalamessa F. Akutní toxicita dvou pyrethroidů, permethrinu a cypermethrinu u novorozenců a dospělých potkanů. Arch Toxicol 1993; 67: 510-13.
- Barrueco C, Herrera A, Caballo C, et al. Indukce strukturálních chromozomálních aberací v kulturách lidských lymfocytů a CHO buňkách permethrinem. Teratog Karcinog Mutagen 1994; 14: 31-8.
- Santoni G, Cantalamessa F, Spreghini E, et al. Změny distribuce a funkcí T buněk u prenatálně vystavených potkanů cypermethrinem: možné zapojení katecholaminů. Toxikologie 1999; 138: 175-87.
Leave a Reply