Virové Latence: Dolů, ale ne ven
Když si představit, viry skrývají z vašeho imunitního systému, může si myslíte, herpes simplex virus, zodpovědný za opary a genitální herpes nebo varicella-zoster virus, který způsobuje pásový opar. Tyto viry mohou přetrvávat po celá desetiletí ve stavu podobném hibernaci známém jako latence a vyhnout se detekci naším imunitním systémem (Kennedy et al ., 2015). Latentní viry se někdy mohou probudit a začít se znovu replikovat, což způsobuje příznaky a šíří infekci (Lieberman, 2016).
virus lidské imunodeficience (HIV) je podobně mistrovským umělcem. Vytváří latentní rezervoár na počátku infekce, což umožňuje viru vyhnout se imunitnímu systému a dlouhodobě přežít. Lidé žijící s HIV užívají denně léky známé jako kombinovaná antiretrovirová terapie (nebo ART), aby se zabránilo replikaci viru. Umění však není lékem, protože se nezaměřuje na viry, které jsou již latentní. Tyto léky jsou proto podávány po celou dobu života jednotlivce: zastavení léčby, a to i po dobu několika týdnů, umožní latentním virům reaktivovat a oživit aktivní infekci. Lidé s HIV mohou očekávat, že budou mít dlouho, zdravý život kvůli umění, ale v jejich těle budou vždy přítomny latentní viry.
nalezení léku na HIV vyžaduje schopnost eliminovat nebo kontrolovat latentní virovou rezervoár. K dosažení tohoto cíle je však třeba ještě vyřešit některé klíčové otázky. Jak, kdy a kde HIV stanoví latenci? Jaká je velikost latentní nádrže a nejlepší způsob, jak ji měřit? Co spouští reaktivaci latentních virů? Nyní, v eLife, Mil Davenport, Brandon Keele a jeho kolegové z University of New South Wales a Frederick Národní Laboratoř pro Výzkum Rakoviny – včetně Mykola Pinkevych jako první autor – zpráva, když latentní nádrž je usazena v non-lidských primátů model HIV a kolik z nádrže může být reaktivován (Pinkevych et al., 2019).
V této studii, tým infikovaných makaků rhesus s opičí imunodeficience (SIV), předchůdce virus, který je endemický v Afrických opic a geneticky podobné HIV (Williams a Burdo, 2009). V určitém okamžiku v průběhu 20. století, SIV skočil z primátů na člověka; tento cross-druh přenosu události, spolu s rychlým vývojem, umožnily virus efektivně šířit do lidí a vytvořit probíhající pandemie HIV (Keele et al., 2006).
Pinkevyč et al. začalo infikováním makaků rhesus s upraveným SIV obsahujícím více než 10 000 jedinečných randomizovaných sekvencí DNA; po sekvenci umožňují tyto „čárové kódy“ identifikovat jednotlivé viry (Fennessey et al., 2017). Opice byly poté léčeny antiretrovirovou terapií 4, 10 nebo 27 dní po infekci. Tyto intervaly simulují akutní (4 dny), časné (10 dní) nebo pozdní intervenci (27 dní) s ART u lidí. Léky byly podávány přibližně rok a virus byl zcela potlačen u všech zvířat. Léčba byla poté zastavena a latentní virus se mohl znovu aktivovat. Pomocí genetického sekvenování a matematického modelování tým určil velikost latentního rezervoáru SIV a způsob jeho reaktivace.
V opice, začíná léčení čtyři dny po infekci neměl blokovat vznik latentní nádrž, ale snížit jeho velikost přibližně 100-krát ve srovnání s pozdější UMĚNÍ zahájení řízení. Podobně lidé, kteří začnou ART během několika dní po získání HIV, mají extrémně malý rezervoár ve srovnání s těmi, kteří zahájí léčbu později (Luzuriaga et al ., 2015; Henrich et al., 2017). Navzdory těmto velkým rozdílům v celkové velikosti nádrže, jakmile byl ART zastaven, se latentní viry reaktivovaly podobným tempem u akutních, časných a pozdně léčených zvířat (Obrázek 1). Pinkevyč a kol. proto dospějte k závěru, že většina virů, které mají potenciál reaktivovat, stanoví latenci brzy po infekci.
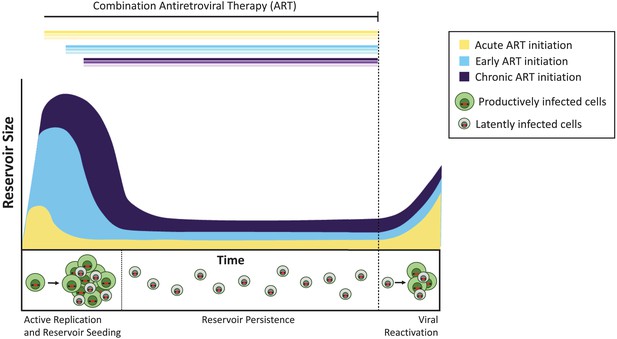
načasování antiretrovirové terapie ovlivňuje velikost latentního rezervoáru.
bez léčby buňky infikované aktivně se replikujícím virem (produktivně infikované buňky; zobrazené zeleně) vytvářejí infekční viry. Menšina infikovaných buněk obsahuje viry, které mohou přetrvávat donekonečna jako latentní rezervoár (latentně infikované buňky; zobrazeny šedě), a tyto viry mohou být později reaktivovány. Léčba během akutní fáze infekce (to znamená, že během dnů nebo týdnů od primární infekce; žlutá křivka) výsledky v menší latentní nádrž, než když je léčba zahájena časně (do šesti měsíců od infekce, světle modrá), nebo v průběhu chronické infekce (déle než 6 měsíců od infekce, fialová). Pokud je léčba zastavena (přerušovaná čára), virus reaktivuje z těchto nádrží na podobné úrovni oživit aktivní infekce a re-seed latentní nádrž.
prozkoumat, proč načasování léčby nezdálo se, že vliv frekvence reaktivace, tým měří úroveň genetické mutace v latentní viry. Pokud viry se hromadí více škodlivých mutací, čím déle jsou aktivně replikaci v těle, to by naznačují, zvířata obdržení opožděné UMĚNÍ mohl nést větší podíl latentní viry, které jsou vadné, a nemůže probudit. Tým však zjistil, že většina virů (více než 80%) byla geneticky neporušená u všech zvířat, bez ohledu na to, kdy byla léčba zahájena. To je zcela jiné, co se stane s infekcí HIV u lidí, kde většinu latentních virů obsahují významné genetické mutace a delece, odcházející jen malý zlomek (mezi 2% a 11%), které jsou schopné reaktivace (Ho et al., 2013; Bruner a kol., 2019).
nedávná studie, která hodnotila dynamiku rezervoáru HIV u lidí na stabilním ART, identifikovala další rozpor mezi tímto modelem SIV a latencí HIV u lidí. Přes pokračující ART, latentní HIV se může někdy spontánně reaktivovat a viry se na krátkou dobu detekují v krvi. U lidí, tyto virové ‚tečky‘ jsou fylogeneticky souvisí s virovou nádrž založena nejen na počáteční infekce, ale celé roky neléčené infekci (Jones et al., 2018). Důvody, které jsou základem těchto rozdílů, nejsou dobře pochopeny a představují důležité oblasti pro probíhající výzkum.
navzdory rozdílům mezi nehumánními modely primátů a infekcí HIV u lidí, práce Pinkevych et al. potvrzuje, že virová latence je stanovena velmi brzy po infekci. Tyto výsledky naznačují, že antiretrovirová léčba by měla být zahájena co nejdříve, aby se zvládla infekce HIV a snížila se velikost latentního rezervoáru. O tom, jak je latence HIV stanovena a udržována, je stále mnoho známo, zejména při léčbě; modely SIV však zůstanou důležitým nástrojem k pochopení toho, jak vymýtit latentní rezervoár.
Leave a Reply