Morula Entwicklung
Google Übersetzen – wählen Sie Ihre Sprache aus der Liste unten dargestellt ist (dies öffnet eine neue, externe Seite)
العربية | català | 中文 | 中國傳統的 | français | Deutsche | עִברִית | हिंदी | bahasa Indonesia | italiano | 日本語 | 한국어 | မြန်မာ | Pilipino | Polskie | português | ਪੰਜਾਬੀ ਦੇ | Română | русский / Español / Swahili / Svensk / ไทร | Türkçe | اردو / वיִדיש / tiếng việT Diese externen Übersetzungen sind automatisiert und können nicht korrekt sein. (Mehr? Über Übersetzungen)
Einführung
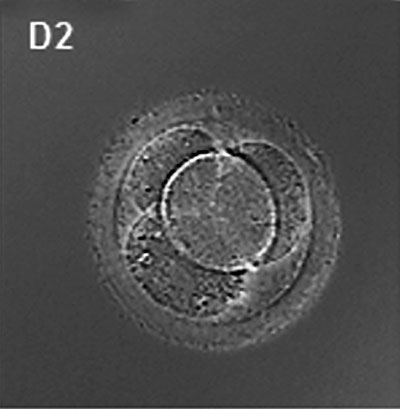
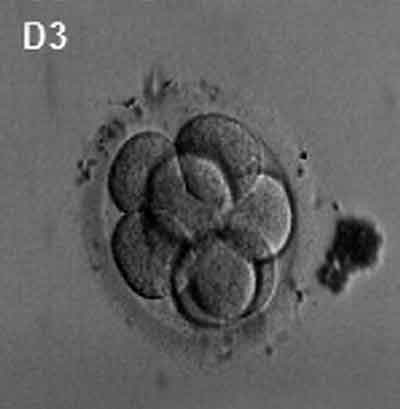
(Lateinisch, Morula = Maulbeere) Ein frühes Stadium in der Entwicklung nach der Befruchtung, wenn sich Zellen schnell mitotisch geteilt haben, um eine feste Masse von Zellen (12-15 Zellen) mit einem „maulbeerartigen“ Aussehen zu erzeugen. Auf dieses Stadium folgt die Bildung eines Hohlraums in diesem Blastozystenstadium der Zellmasse.Ein Schlüsselereignis vor der Morula-Bildung ist die „Verdichtung“, bei der der 8-Zell-Embryo Veränderungen in der Zellmorphologie und der Zell-Zell-Adhäsion erfährt, die die Bildung dieser festen Zellkugel initiieren.
Beim Menschen tritt das Morula-Entwicklungsstadium in den ersten Tagen der ersten Woche nach der Befruchtung (GA-Woche 3) auf und wird als Carnegie-Stadium 2 beschrieben. Auf dieses Stadium folgt die Bildung eines Hohlraums, des Blastocoels, der die Bildung der Blastozyste definiert.

ART-Präimplantations-Blastomerbiopsie
|
In der assistierten Reproduktionstechnologie ist das Morula-Stadium, wenn einer der frühesten pränatalen diagnostischen Tests durchgeführt werden kann, indem eine einzelne Zelle (Blastomer) entfernt und eine genetische Diagnose durchgeführt wird auf seiner DNA. |
Molekular – In der Maus wurde während des Übergangs vom Morula- zum Blastozystenstadium gezeigt, dass die Differenzierung der inneren Zellmasse (ICM) und des Trophektoderms (TE) durch den Hippo-Signalweg reguliert wird.
Morula Links: Morula / Carnegie Stadium 2 / Mitose / Blastozyste / Befruchtung / Woche 1 / Vorlesung – Woche 1 / Kategorie:Carnegie Stadium 2 / Kategorie:Morula
Einige neuere Erkenntnisse
- Wirkung der Herunterregulierung des Hippo-Signalwegs in YAP1- und LATS2-Transkripten auf die frühe Entwicklung und Genexpression, die an der Differenzierung von Schweineembryonen beteiligt ist „Bei der Mausentwicklung wird die Differenzierung der inneren Zellmasse (ICM) und des Trophektoderms (TE) während des Übergangs vom Morula- zum Blastozystenstadium durch den Hippo-Signalweg reguliert; die Funktionen des Hippo-Signalwegs bei der Embryogenese von Schweinen untersucht. In der vorliegenden Studie untersuchten wir die Genexpressionsmuster der Hippo-Pathway-Mitglieder yes-associated Protein 1 (YAP1) und Large Tumor Suppressor 2 (LATS2) und die Funktionen dieser Gene während der Präimplantationsentwicklung bei Schweinen mittels RNA-Interferenz. Sowohl die YAP1- als auch die LATS2-mRNA-Spiegel waren in den in vitro gereiften Oozyten und Embryonen im 1-Zellstadium hoch und fielen mit der Entwicklung progressiv ab. Die YAP1-Kernlokalisation wurde im Morula- und Blastozystenstadium nachgewiesen. Die Herunterregulation von YAP1 oder LATS2 hemmte die Präimplantationsentwicklung bei Schweinen und beeinflusste die Expressionsniveaus der Homöobox 1 (OCT-4) der POU-Klasse 5 und des SRY-verwandten HMG-Box-Gens 2 (SOX2), Transkriptionsfaktoren, die für die ICM / TE-Differenzierung notwendig sind. Zusammengenommen sind YAP1 und LATS2 essentiell für die Präimplantationsentwicklung von Schweinen, und es ist möglich, dass der Hippo-Signalweg eine wichtige Rolle bei der ICM / TE-Segregation von Schweinen spielt.“
- Diversity of human and mouse homeobox gene expression in development and adult tissues „8-cell to morula, 12 eutherian-spezifische Homeobox-Gene, die außerhalb von Reproduktionsgeweben oder des Embryos nicht nachweisbar sind (RHOXF2, RHOXF2B, CPHX1, CPHX2, DPRX, LEUTX, TPRX1, TPRX2, ARGFX, NANOGNB, DUXA, DUXB). Hox

Diese Tabelle ermöglicht eine automatisierte Computersuche der externen PubMed-Datenbank unter Verwendung des aufgelisteten Textlinks „Suchbegriff“.
- Diese Suche erfordert jetzt einen manuellen Link, da die ursprüngliche PubMed-Erweiterung deaktiviert wurde.
- Die angezeigte Referenzliste spiegelt keine redaktionelle Auswahl des Materials nach Inhalt oder Relevanz wider.
- Verweise erscheinen auch in dieser Liste basierend auf dem Datum der tatsächlichen Seitenansicht.
Referenzen, die auf der restlichen Inhaltsseite und der zugehörigen Diskussionsseite (aufgeführt unter den Unterüberschriften des Veröffentlichungsjahres) aufgeführt sind, enthalten eine redaktionelle Auswahl, die sowohl auf Relevanz als auch auf Verfügbarkeit basiert.
Mehr? Referenzen / Diskussionsseite / Zeitschriftensuche / 2019 Referenzen / 2020 Referenzen
Suchbegriff: Morula Development | Morula Compaction | Morula Blastomere Division | Morula Hippo /
Diese Papiere erschienen ursprünglich in der Some Recent Findings table, wurden aber mit zunehmender Länge in diese zusammenklappbare Tabelle gemischt.
Siehe auch die Diskussionsseite für andere Referenzen, die nach Jahr und Referenzen auf dieser aktuellen Seite aufgelistet sind.
- Par-aPKC-abhängige und -unabhängige Mechanismen steuern kooperativ die Zellpolarität, die Hippo-Signalisierung und die Zellpositionierung in Mausembryonen im 16-Zellstadium „Bei Präimplantationsembryonen von Mäusen spielt der Hippo-Signalweg eine zentrale Rolle bei der Regulierung des Schicksals des Trophektoderms (TE) und der inneren Zellmasse (ICM). In frühen Blastozysten mit mehr als 32 Zellen steuert das Par-aPKC-System die Polarisation der äußeren Zellen entlang der apikobasalen Achse, und die Zellpolarität unterdrückt die Hippo-Signalisierung.“ Hippo / Maus
- Nichtinvasive Bildgebung menschlicher Embryonen vor der Aktivierung des embryonalen Genoms sagt die Entwicklung bis zum Blastozystenstadium voraus „Wir berichten über Studien zur Präimplantationsentwicklung menschlicher Embryonen, die Zeitrafferbildanalyse und Genexpressionsprofil korrelieren. Durch die Untersuchung einer großen Anzahl von Zygoten aus der In-vitro-Fertilisation (IVF) stellen wir fest, dass der Erfolg beim Fortschreiten zum Blastozystenstadium mit >93% Sensitivität und Spezifität vorhergesagt werden kann, indem drei dynamische, nichtinvasive Bildgebungsparameter am Tag 2 nach der Befruchtung vor der Aktivierung des embryonalen Genoms (EGA) gemessen werden.“
- Funktionelle Genomik von menschlichen Embryonen im 5- bis 8-Zellstadium durch Blastomer-Einzelzell-cDNA-Analyse „Neunundvierzig Blastomere von menschlichen Embryonen im 5- bis 8-Zellstadium wurden nach einem effizienten Einzelzell-cDNA-Amplifikationsprotokoll untersucht, um eine Vorlage für die High-Density-Microarray-Analyse bereitzustellen. Die zuvor beschriebenen Marker, die für die innere Zellmasse (ICM) (n = 120), die Stammheit (n = 190) und das Trophektoderm (TE) (n = 45) charakteristisch sind, wurden analysiert und ein Housekeeping-Muster von 46 Genen wurde festgestellt. …Zusammenfassend zeigt die globale Einzelzell-cDNA-Amplifikations-Microarray-Analyse der menschlichen Embryonen im 5- bis 8-Zellstadium, dass das Blastomerschicksal nicht an ICM oder TE gebunden ist.“
Filme
|
Morula Modell Seite / Wiedergabe
|
Zygote Mitosis Page | Play
|
Early Division Page | Play
|
Parental Genomes Page | Play
|
Mouse Blastocyst Page | Play
|
Movies
Compaction
- E-cadherin mediated adhesion initiates at compaction at the 8-cell stage
- regulated post-translationally via protein kinase C and other signalling molecules
Blastomere Division

Eine In-vitro-Studie zur Entwicklung menschlicher Blastozysten zeigte, dass sich diejenigen Blastomere, die sich anfänglich schnell teilen, eher zum Blastozystenstadium entwickeln.Eine aktuelle Studie an Mäusen zeigte, dass es keine spezifische Orientierung der mitotischen Spindel während der Zellteilung im Übergang von 8 zu 16 Zellen gab. Dies deutet auf kein vorbestimmtes Spaltmuster (vorgemustert) im 8-Zellstadium hin und wird nur durch das Ausmaß der Zellrundung während der Mitose moduliert. Bei anderen Arten wie dem Wurm C.elegans und Ascidians haben spezifische Muster der Spindelorientierung aus dem Zygotenstadium.
Modell der menschlichen Morula-Entwicklung
Die folgende Abbildung stammt aus einer kürzlich durchgeführten Studie mit Video- und Genanalyse der In-vitro-Entwicklung des Menschen in Woche 1 nach der Befruchtung.
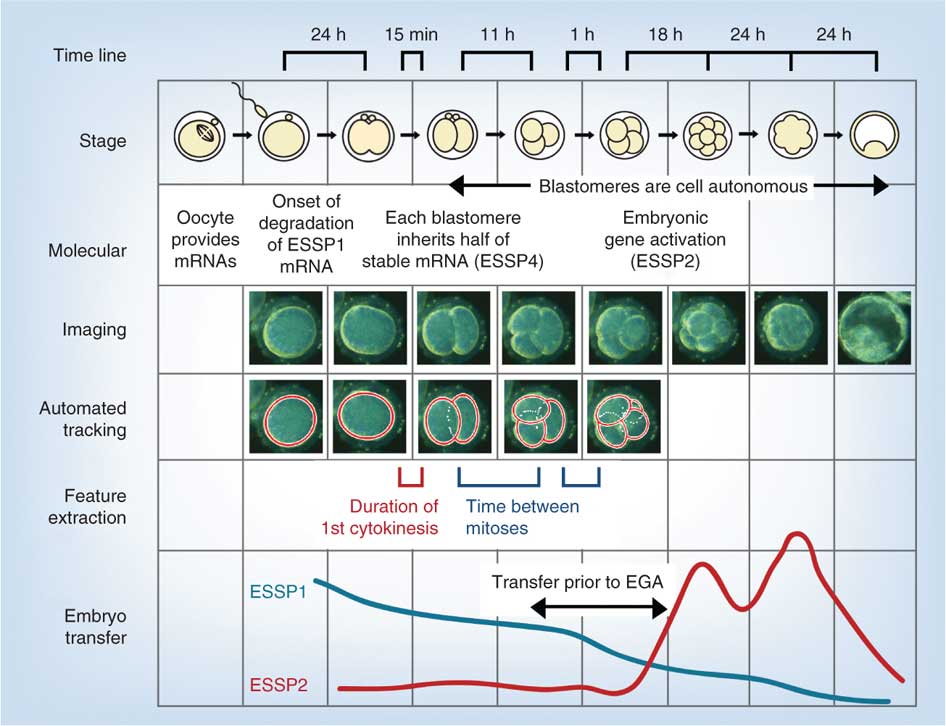
- EGA – Aktivierung des embryonalen Genoms
- ESSP – spezifisches Muster im Embryonalstadium, vier einzigartige spezifische Muster im Embryonalstadium (1-4)
Links: Abbildung mit Legende
Morula in Other Species
Mouse Morula
Bei der Maus wurde gezeigt, dass die Differenzierung der inneren Zellmasse (ICM) und des Trophektoderms (TE) während des Übergangs vom Morula- zum Blastozystenstadium durch den Hippo-Signalweg reguliert wird.
-

4 cell morula stage development
-

Sox2 expression
-

Early gene expression
-

Early gene expression
-

Early gene expression
-

Early genexpression
Links: Mausentwicklung
Seeigel Morula

Seeigel frühen embryo spaltung muster (SDB Galerie Bilder)
Links: Seeigel Entwicklung
Bovine Morula
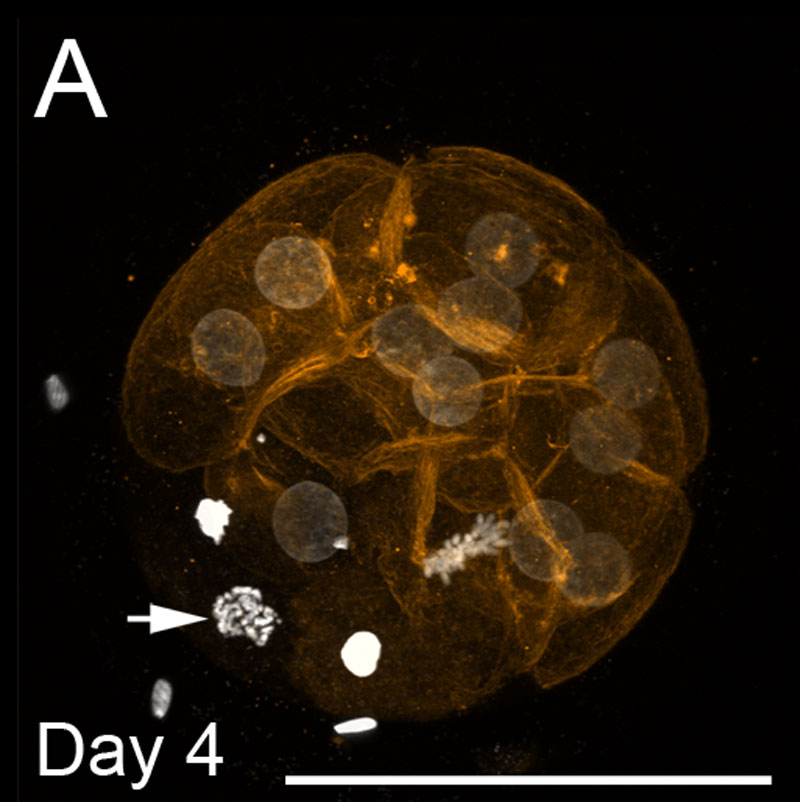
Rindermorula
- Bild zeigt DNA-Färbung (weiß) und f-Aktin-Filamente (orange) am Tag 4. Skalenbalken repräsentieren 100 µm.
- Blassfärbende runde Kerne befinden sich in der Interphase.
- Pfeil zeigt Einzelkern an Prophase.
- Ein einzelner Kern ist an der Metaphase zu sehen.
- Kondensierte helle Kerne sind apoptotisch.
Links: Rinderentwicklung / Mitose
Morula-Biopsie

Biopsie kompakter Embryonen im Morula-Stadium
- (A) Ein kompakter Embryo im Morula-Stadium vor der Biopsie.
- (B–G) Schritte der Biopsie.
- (H) Ein Embryo bei 2 h nach der Biopsie.
Links: Pränataldiagnostik / Assistierte Reproduktionstechnik
- 1.0 1.1 Zhang P., Zucchelli M., Bruce S., Hambiliki F., Stavreus-Evers A., Levkov L., Skottman H., Kerkelä E., Kere J. & Hovatta O. (2009). Transkriptomprofilierung der menschlichen Präimplantationsentwicklung. Plus EINS , 4, e7844. PMID: 19924284 DOI.
- Milachich T. (2014). Neue Fortschritte bei Präimplantations- und pränatalen genetischen Screenings und nichtinvasiven Tests als potenzieller Prädiktor für den Gesundheitszustand von Babys. Biomed Res Int , 2014, 306505. PMID: 24783200 DOI.
- 3.0 3.1 Hirate Y, Hirahara S, Inoue K, Kiyonari H, Niwa H & Sasaki H. (2015). Par-aPKC-abhängige und unabhängige Mechanismen steuern kooperativ die Zellpolarität, Hippo-Signalisierung und Zellpositionierung in Mausembryonen im 16-Zellstadium. Dev. Wachstum unterscheiden. , 57, 544-56. PMID: 26450797 DOI.
- 4,0 4,1 4,2 Emura N, Saito Y, Miura R & Sawai K. (2020). Wirkung der Herunterregulierung des Hippo-Signalwegs in YAP1- und LATS2-Transkripten auf die frühe Entwicklung und Genexpression, die an der Differenzierung von Schweineembryonen beteiligt sind. Zelle neu programmieren , , . PMID: 32150685 DOI.
- Dunwell TL & Niederlande PW. (2016). Vielfalt der menschlichen und Maus homeobox Genexpression in der Entwicklung und adulten Geweben. BMC Dev. Biol. , 16, 40. PMID: 27809766 DOI.
- 6,0 6,1 Wong CC, Loewke KE, Bossert NL, Behr B, De Jonge CJ, Bär TM & Reijo Pera RA. (2010). Die nicht-invasive Bildgebung menschlicher Embryonen vor der Aktivierung des embryonalen Genoms sagt die Entwicklung bis zum Blastozystenstadium voraus. Nat. In: Biotechnol. , 28, 1115-21. PMID: 20890283 DOI.
- Galán A, Montaner D, Póo MICH, Valbuena D, Ruiz V, Aguilar C, Dopazo J & Simón C. (2010). Funktionelle Genomik von menschlichen Embryonen im 5- bis 8-Zellstadium durch Blastomer-Einzelzell-cDNA-Analyse. Plus EINS , 5, e13615. PMID: 21049019 DOI.
- 8,0 8,1 Dard N, Louvet-Vallée S & Maro B. (2009). Orientierung der mitotischen Spindeln während des Übergangs von 8 zu 16 Zellen in Mausembryonen. Plus EINS , 4, e8171. PMID: 19997595 DOI.
- Fenwick J, Platteau P, Murdoch AP & Herbert M. (2002). Die Zeit von der Insemination bis zur ersten Spaltung sagt die Entwicklungskompetenz menschlicher Präimplantationsembryonen in vitro voraus. Summen. Reprod. , 17, 407-12. PMID: 11821286
- Leidenfrost S., Boelhauve M., Reichenbach M., Güngör T., Reichenbach H., Sinowatz F., Wolf E. & Habermann FA. (2011). Zellstillstand und Zelltod in der Präimplantationsentwicklung von Säugetieren: Lehren aus dem Rindermodell. Plus EINS , 6, e22121. PMID: 21811561 DOI.
- Zakharova EE, Zaletova VV & Krivokharchenko ALS. (2014). Biopsie von menschlichen Embryonen im Morula-Stadium: Ergebnis von 215 IVF / ICSI-Zyklen mit PGS. PLoS ONE , 9, e106433. PMID: 25191937 DOI.
Bewertungen
Coticchio G, Lagalla C, Sturmey R, Pennetta F & Borini A. (2019). Die rätselhafte Morula: Mechanismen der Entwicklung, Bestimmung des Zellschicksals, Selbstkorrektur und Implikationen für die KUNST. Summen. Reprod. Aktualisieren , 25, 422-438. PMID: 30855681 DOI.
Artikel
Bessonnard S, Mesnard D & Constam DB. (2015). PC7 und die verwandten Proteasen Furin und Pace4 regulieren die E-Cadherin-Funktion während der Blastozystenbildung. In: J. Cell Biol. , 210, 1185-97. PMID: 26416966 DOI.
Dzamba BJ, Jakab KR, Marsden M, Schwartz MA & DeSimone DW. (2009). Cadherin-Adhäsion, Gewebespannung und nichtkanonische Wnt-Signalisierung regulieren die Organisation der Fibronektin-Matrix. Dev. Zelle , 16, 421-32. PMID: 19289087 DOI.
Santos J, Pereira CF, Di-Gregorio A, Fichte T, Erle O, Rodriguez T, Azuara V, Merkenschlager M & Fischer AG. (2010). Unterschiede in den epigenetischen und reprogrammierenden Eigenschaften pluripotenter und extraembryonaler Stammzellen implizieren die Chromatinumgestaltung als wichtiges frühes Ereignis im sich entwickelnden Mausembryo. Epigenetik Chromatin , 3, 1. PMID: 20157423 DOI.
Suche PubMed
Suche Pubmed: morula Entwicklung | blastomere Entwicklung /
Glossar Links Glossar: A | B | C | D | E |F |G |H | I |J | K | L |M | N |O | P | Q | R | S | T | U | V | W | X | Y | Z | Zahlen | Symbole / Begriff Link
Zitieren Sie diese Seite: Hill, M.A. (2021, März 24) Embryology Morula Development. Abgerufen von https://embryology.med.unsw.edu.au/embryology/index.php/Morula_Development
Leave a Reply