Mórula Desarrollo
el traductor de Google – seleccione su idioma en la lista que se muestra a continuación (se abrirá una nueva página externa)
العربية | català | 中文 | 中國傳統的 | français | Deutsche | עִברִית | हिंदी | bahasa Indonesia | italiano | 日本語 | 한국어 | မြန်မာ | Filipino | Polskie | português | ਪੰਜਾਬੀ ਦੇ | Română | русский | Español | Swahili | Svensk | ไทย | Türkçe | اردو | ייִדיש | Tiếng Việt These external translations are automated and may not be accurate. (More? Acerca de las traducciones)
Introducción
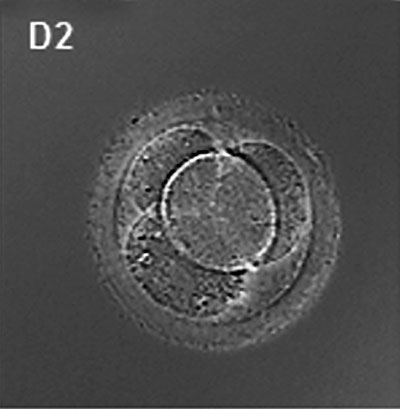
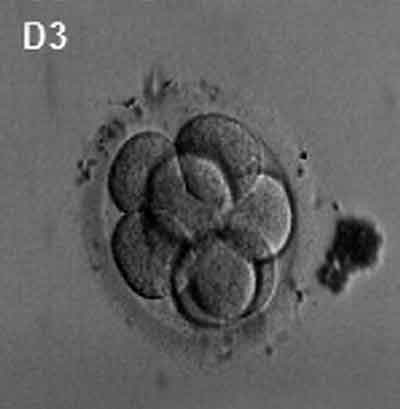
(Latín, mórula = morera) Una etapa temprana en el desarrollo post-fertilización cuando las células se han dividido mitóticamente rápidamente para producir una masa sólida de células (12-15 células) con una apariencia de «morera». Esta etapa es seguida por la formación de una cavidad en esta etapa de blastocisto de masa celular.
Un evento clave antes de la formación de la mórula es la «compactación», donde el embrión de 8 células experimenta cambios en la morfología celular y la adhesión celular-celular que inicia la formación de esta bola sólida de células.
En los seres humanos, la etapa de desarrollo de la mórula se produce durante los primeros días de la primera semana después de la fertilización (semana 3 de AG) y se describe como la etapa 2 de Carnegie. Esta etapa es seguida por la formación de una cavidad, el blastocele, que define la formación del blastocisto.

Preimplantación ART biopsia de blastómero
|
En la Tecnología de Reproducción Asistida, la etapa de mórula es cuando se puede realizar una de las pruebas de diagnóstico prenatal más tempranas, mediante la extracción de una sola célula (blastómero) y la realización de un diagnóstico genético en su ADN. |
– Molecular En el ratón, durante la transición de mórula a la etapa de blastocisto, la diferenciación de la masa celular interna (ICM) y trophectoderm (TE) ha demostrado ser regulada por la vía de Hipona.Enlaces de Morula: morula / Carnegie etapa 2 / mitosis / blastocisto / fertilización / Semana 1 / Semana de conferencias 1 / Categoría: Carnegie Etapa 2 / Categoría:Mórula
Algunos Hallazgos Recientes
- Efecto de la Regulación a la Baja de las Transcripciones de los Miembros de la Vía Hipopótamo YAP1 y LATS2 en el Desarrollo Temprano y la Expresión Génica Involucrada en la Diferenciación en Embriones Porcinos «En el desarrollo de ratones, la diferenciación de la masa celular interna (MIC) y el trofectodermo (TE) durante la transición de la mórula a la etapa de blastocisto está regulada por la vía hipopótamo; sin embargo, las funciones de la vía hipopótamo en la embriogénesis porcina no se han investigado. En el presente estudio, examinamos los patrones de expresión génica de la proteína 1 asociada a la vía hipopótamo (YAP1) y el supresor tumoral grande 2 (LATS2) y las funciones de estos genes durante el desarrollo preimplantacional porcino utilizando interferencia de ARN. Los niveles de ARNm de YAP1 y LATS2 se mostraron altos en los ovocitos madurados in vitro y embriones en estadio de 1 célula y disminuyeron progresivamente con el desarrollo. La localización nuclear de YAP1 se detectó en las etapas de mórula y blastocisto. La regulación a la baja de YAP1 o LATS2 inhibió el desarrollo preimplantacional porcino y afectó los niveles de expresión de la homeobox 1 de clase 5 de POU (OCT-4) y el gen 2 de la HMG-box relacionado con SRY (SOX2), factores de transcripción necesarios para la diferenciación ICM/TE. En conjunto, YAP1 y LATS2 son esenciales para el desarrollo preimplantacional porcino, y es posible que la vía hipopótamo tenga un papel importante en la segregación de ICM/TE porcino.»
- Diversidad de la expresión génica de la homeobox humana y de ratón en el desarrollo y en los tejidos adultos » 8 células a mórula, 12 genes homeobox específicos de euteria no detectables fuera de los tejidos reproductivos o del embrión (RHOXF2, RHOXF2B, CPHX1, CPHX2, DPRX, LEUTX, TPRX1, TPRX2, ARGFX, NANOGNB, DUXA, DUXB). Hox

Esta tabla permite una búsqueda automatizada por computadora de la base de datos externa de PubMed utilizando el enlace de texto «Término de búsqueda» listado.
- Esta búsqueda ahora requiere un enlace manual, ya que la extensión PubMed original se ha desactivado.
- La lista de referencias mostrada no refleja ninguna selección editorial de material basada en el contenido o la relevancia.
- Las referencias también aparecen en esta lista en función de la fecha de visualización real de la página.
Las referencias que aparecen en el resto de la página de contenido y en la página de discusión asociada (que se enumeran en los subtítulos del año de publicación) incluyen una selección editorial basada en la relevancia y la disponibilidad.
Más? Referencias | Página de discusión / Búsquedas en revistas / Referencias de 2019/Referencias de 2020
Término de búsqueda: Desarrollo de Morula | Compactación de Morula | División de Blastómeros de Morula | Hipopótamo de Morula /
Estos artículos aparecieron originalmente en la tabla de Algunos hallazgos recientes, pero a medida que la lista creció en longitud, ahora se han barajado a esta tabla plegable.
Vea también la Página de Discusión para otras referencias listadas por año y Referencias en esta página actual.
- Mecanismos independientes y dependientes de Par-aPKC controlan cooperativamente la polaridad celular, la señalización de hipopótamos y el posicionamiento celular en embriones de ratón de 16 células «En embriones de ratón preimplantación, la vía de señalización de hipopótamos desempeña un papel central en la regulación de los destinos del trofectodermo (TE) y la masa celular interna (MIC). En los primeros blastocistos con más de 32 células, el sistema Par-aPKC controla la polarización de las células externas a lo largo del eje apicobasal, y la polaridad celular suprime la señalización hipopótamo.»Hipopótamo / ratón
- La obtención de imágenes no invasivas de embriones humanos antes de la activación del genoma embrionario predice el desarrollo hasta la etapa de blastocisto «Reportamos estudios de desarrollo de embriones humanos antes de la implantación que correlacionan el análisis de imágenes a intervalos de tiempo y el perfil de expresión génica. Al examinar un gran conjunto de cigotos de la fertilización in vitro (FIV), encontramos que el éxito en la progresión a la etapa de blastocisto se puede predecir con >93% de sensibilidad y especificidad midiendo tres parámetros de imagen dinámicos no invasivos para el día 2 después de la fertilización, antes de la activación del genoma embrionario (EGA).»
- Genómica funcional de embriones humanos en estadio de 5 a 8 células mediante análisis de ADNc unicelular de blastómeros » Se han investigado cuarenta y nueve blastómeros de embriones humanos de 5 a 8 células siguiendo un protocolo de amplificación de ADNc unicelular eficiente para proporcionar una plantilla para el análisis de microarray de alta densidad. Se analizaron los marcadores descritos anteriormente, característicos de la Masa Celular Interna (MIC) (n = 120), el tallo (n = 190) y el Trofectodermo (TE) (n = 45), y se estableció un patrón de limpieza de 46 genes. …En resumen, el análisis de microarray de amplificación de ADNc unicelular global de embriones humanos en estadios de 5 a 8 células revela que el destino de los blastómeros no está comprometido con ICM o TE.»
Películas
|
Mórula Modelo Página | Play
|
Zygote Mitosis Page | Play
|
Early Division Page | Play
|
Parental Genomes Page | Play
|
Mouse Blastocyst Page | Play
|
Movies
Compaction
- E-cadherin mediated adhesion initiates at compaction at the 8-cell stage
- regulated post-translationally via protein kinase C and other signalling molecules
Blastomere Division

En un estudio in vitro de desarrollo de blastocitos humanos, se observó que los blastómeros que inicialmente se dividen rápidamente tienen más probabilidades de convertirse en estadio de blastocitos.
Un estudio reciente en ratones mostró que no había una orientación específica del huso mitótico durante la división celular en la transición de 8 a 16 estadios celulares. Esto sugiere que no hay un patrón de escisión predeterminado (preformado) en la etapa de 8 células y solo modulado por el grado de redondeo celular durante la mitosis. En otras especies, como el gusano C.elegans y ascidias, tienen patrones específicos de la orientación del eje de la fase de cigoto.
Modelo de Desarrollo de Mórula Humana
La siguiente figura es de un estudio reciente que utiliza video y análisis genético del desarrollo humano in vitro durante la semana 1 después de la fertilización.
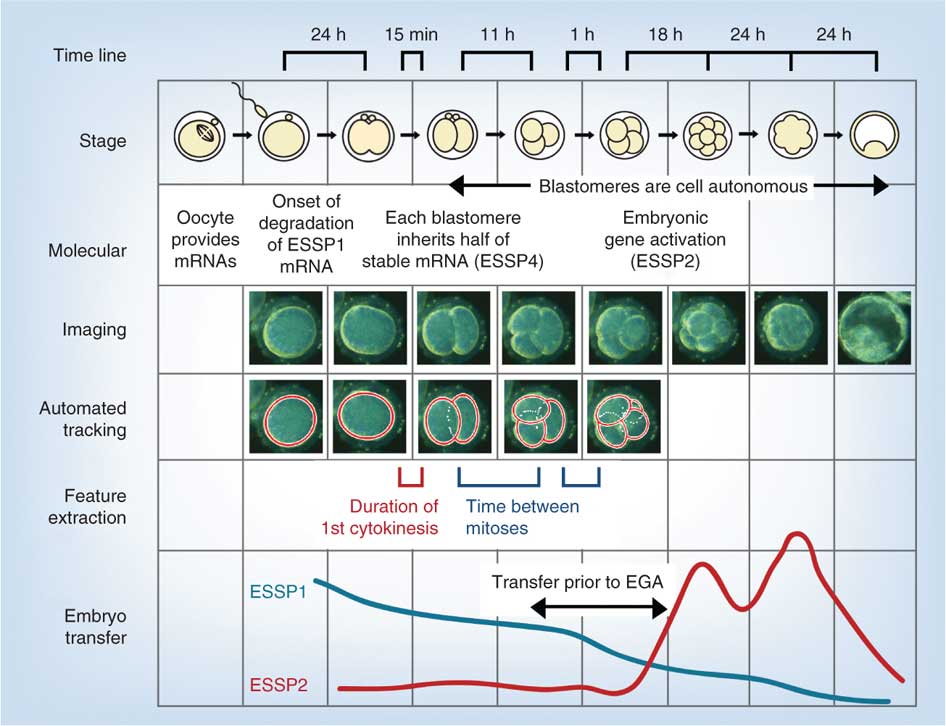
- Activación del genoma embrionario EGA
- ESSP: patrón específico de la etapa embrionaria, cuatro patrones únicos específicos de la etapa embrionaria (1-4)
Enlaces: Figura con leyenda
Mórulas en Otras Especies
Mórula de ratón
En el ratón, durante la transición de la mórula a la etapa de blastocisto, se ha demostrado que la diferenciación de la masa celular interna (MIC) y del trofectodermo (TE) está regulada por la vía hipopótamo.
-

4 cell morula stage development
-

Sox2 expression
-

Early gene expression
-

Early gene expression
-

Early gene expression
-

Early expresión génica
Enlaces: Desarrollo de ratones
Morula de erizo de mar

Patrón de escisión del embrión temprano de erizo de mar (Imágenes de la Galería SDB)
Enlaces: Desarrollo de erizos de mar
Mórula bovina
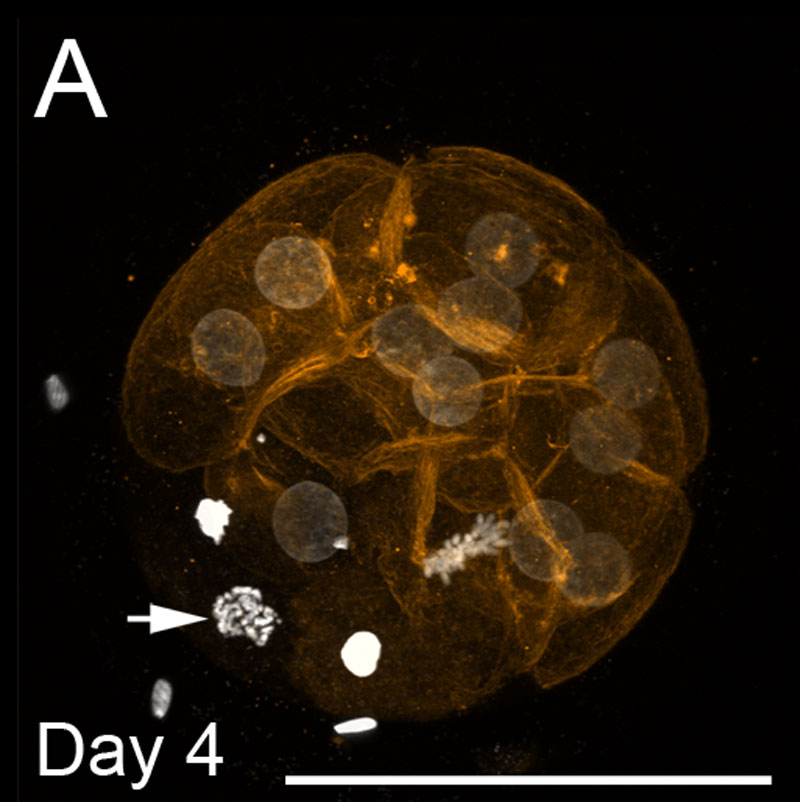
Mórula bovina
- Muestra tinción de ADN (blanco) y filamentos de actina f (naranja) en el día 4. Las barras de escala representan 100 µm.
- Los núcleos redondos de tinción pálida están en interfase.
- La flecha muestra un solo núcleo en la profase.
- Se ve un único núcleo en metafase.
- Los núcleos brillantes condensados son apoptóticos.
Enlaces: Desarrollo bovino / mitosis
Biopsia de mórula

Biopsia de embriones en estadio mórula compacto
- (A) Un embrión en estadio mórula compacto antes de la biopsia.
- (B–G) Pasos de la biopsia.
- (H) Un embrión a las 2 h después de la biopsia.
Enlaces: Diagnóstico Prenatal | Tecnología de reproducción Asistida
- 1.0 1.1 Zhang P, Zucchelli M, Bruce S, Hambiliki F, Stavreus-Evers A, Levkov L, Skottman H, Kerkelä E, Kere J & Hovatta O. (2009). Perfil de transcriptoma del desarrollo humano preimplantacional. PLoS UNO, 4, e7844. PMID: 19924284 DOI.
- Milachich T. (2014). Nuevos avances en el cribado genético preimplantacional y prenatal y las pruebas no invasivas como predictor potencial del estado de salud de los bebés. Biomed Res Int, 2014, 306505. PMID: 24783200 DOI.
- 3.0 3.1 Hirate Y, Hirahara S, Inoue K, Kiyonari H, Niwa H & Sasaki H. (2015). Los mecanismos dependientes e independientes de Par-aPKC controlan de forma cooperativa la polaridad celular, la señalización de hipopótamos y el posicionamiento celular en embriones de ratón de 16 células. Dev. El crecimiento Es Diferente. , 57, 544-56. PMID: 26450797 DOI.
- 4.0 4.1 4.2 Emura N, Saito Y, Miura R & Sawai K. (2020). Efecto de la Regulación a la Baja de las Transcripciones de los Miembros de la Vía Hipopótamo YAP1 y LATS2 en el Desarrollo Temprano y la Expresión Génica Involucrada en la Diferenciación en Embriones Porcinos. Reprogramación Celular , , . PMID: 32150685 DOI.
- Dunwell TL & Holland PW. (2016). Diversidad de la expresión génica homeobox humana y de ratón en el desarrollo y tejidos adultos. BMC Dev. Biol. , 16, 40. PMID: 27809766 DOI.
- 6.0 6.1 Wong CC, Loewke KE, Bossert NL, Behr B, De Jonge CJ, Baer TM & Reijo Pera RA. (2010). La obtención de imágenes no invasivas de embriones humanos antes de la activación del genoma embrionario predice el desarrollo hasta la etapa de blastocisto. NAT. Biotechnol. , 28, 1115-21. PMID: 20890283 DOI.
- Galán A, Montaner D, Póo ME, Valbuena D, Ruiz V, Aguilar C, Dopazo J & Simón C. (2010). Genómica funcional de embriones humanos en estadios de 5 a 8 células mediante análisis de ADNc unicelular de blastómeros. PLoS UNO, 5, e13615. PMID: 21049019 DOI.
- 8.0 8.1 Dard N, Louvet-Vallée S & Maro B. (2009). Orientación de los husillos mitóticos durante la transición de 8 a 16 células en embriones de ratón. PLoS UNO, 4, e8171. PMID: 19997595 DOI. Fenwick J, Platteau P, Murdoch AP & Herbert M. (2002). El tiempo transcurrido desde la inseminación hasta la primera escisión predice la capacidad de desarrollo de los embriones humanos antes de la implantación in vitro. Zumbido. Reproche. , 17, 407-12. PMID: 11821286
- Leidenfrost S, Boelhauve M, Reichenbach M, Güngör T, Reichenbach HD, Sinowatz F, Wolf E & Habermann FA. (2011). Detención y muerte celular en el desarrollo preimplantacional de mamíferos: lecciones del modelo bovino. PLoS UNO, 6, e22121. PMID: 21811561 DOI.
- Zakharova EE, Zaletova VV & Krivokharchenko AS. (2014). Biopsia de embriones humanos en estadio de mórula: resultado de 215 ciclos de FIV/ICSI con GPS. PLoS UNO, 9, e106433. PMID: 25191937 DOI.
Reviews
Coticchio G, Lagalla C, Sturmey R, Pennetta F & Borini A. (2019). The enigmatic morula: mechanisms of development, cell fate determination, self-correction and implications for ART (en inglés). Zumbido. Reproche. Update, 25, 422-438. PMID: 30855681 DOI.
Artículos
Bessonnard S, Mesnard D & Constam DB. (2015). El PC7 y las proteasas relacionadas Furina y Pace4 regulan la función de la E-cadherina durante la formación de blastocitos. J. Cell Biol. , 210, 1185-97. PMID: 26416966 DOI.
Dzamba BJ, Jakab KR, Marsden M, Schwartz MA & DeSimone DW. (2009). La adhesión de cadherina, la tensión tisular y la señalización Wnt no canónica regulan la organización de la matriz de fibronectina. Dev. Celda, 16, 421-32. PMID: 19289087 DOI.
Santos J, Pereira CF, Di-Gregorio A, Spruce T, Alder O, Rodriguez T, Azuara V, Merkenschlager M& Fisher AG. (2010). Las diferencias en las propiedades epigenéticas y de reprogramación de las células madre pluripotentes y extraembrionarias implican el remodelado de la cromatina como un evento temprano importante en el embrión de ratón en desarrollo. Cromatina epigenética, 3, 1. PMID: 20157423 DOI.
Buscar PubMed
Buscar Pubmed: desarrollo de morula | desarrollo de blastómeros /
Enlaces de glosario Glosario: A | B | C | D | E | F | G | H | I | J | K | L | M | N | O | P | Q | R | S | T | U | V | W | X | Y | Z | Números | Símbolos/Enlace de términos
Citar esta página: Hill, M. A. (2021, 24 de marzo) Embryology Desarrollo de Morula. Recuperado de https://embryology.med.unsw.edu.au/embryology/index.php/Morula_Development
Leave a Reply