Lumière sur un Nerf optique pâle
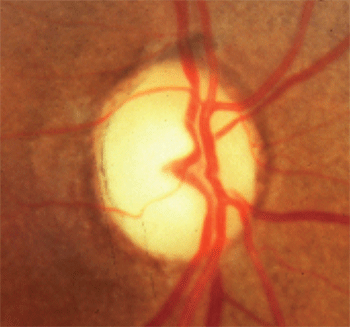
1. Pâleur du disque optique en excès de ventouses.
Diverses insultes peuvent survenir au nerf optique et se manifester ophtalmoscopiquement par une pâleur, une atrophie, des ventouses et des entailles. De loin, l’affliction du nerf optique la plus courante est le glaucome.
Le glaucome présente une atrophie caverneuse très caractéristique, communément appelée « ventouses » ou « entailles ». »Cette neuropathie distinctive se présente avec un élargissement de la coupelle du disque optique — préférentiellement aux régions inférieure et supérieure — avec un motif de ventouses verticales élargi et un compromis ou une oblitération du bord neurorétinal.
Dans cette maladie chronique, il y a généralement une absence de pâleur. Le tissu du bord reste bien perfusé, bien que des lésions focales se produisent sur le bord neurorétinien supérieur et inférieur.
De temps en temps, les patients présenteront des nerfs optiques de type glaucomateux et présenteront des caractéristiques supplémentaires, telles que la pâleur, qui indiquent la présence d’une autre affection entièrement ou d’une entité en plus du glaucome. Il existe également plusieurs entités et situations cliniques dans lesquelles le nerf optique peut être compromis et ressembler superficiellement à un glaucome. Il est impératif de différencier correctement ces neuropathies non glaucomateuses du glaucome.
Y A-t-il une Pâleur De Disque Optique?
Il est parfois difficile d’identifier la pâleur du disque optique lorsque la maladie est subtile, ou qu’il y a des problèmes de médias et de cataracte qui nuisent au jugement. Il peut également être difficile de différencier la véritable pâleur discale des mimiques. Par exemple, après l’extraction de la cataracte, il y a une perte des propriétés atténuantes de la lumière du cristallin naturel. Le disque peut sembler pâle, mais il n’y a pas de dysfonctionnement nerveux — c’est ce qu’on appelle le « pseudopallor pseudophakique”, et peut être assez déconcertant et trompeur.1
Dans les cas unilatéraux, il est utile de photographier chaque disque et de les comparer côte à côte. Ce faisant, la pâleur du disque optique dans un œil peut être plus facilement identifiée, même lorsqu’elle est subtile.
 |
|
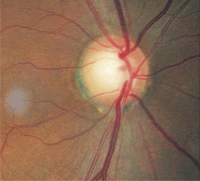
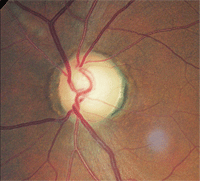
| 2. Pâleur discale relative, O.D. (gauche) par rapport à O.S. (droite). La plus grande pâleur de l’œil gauche indique une atrophie optique. | |
L’atrophie optique, se manifestant par une pâleur du disque optique, existe rarement isolément. En tant que tel, il est impératif de rechercher un dysfonctionnement du nerf optique associé pour séparer les conditions mimétiques de la véritable atrophie optique.
Les associations qui indiqueraient une véritable atrophie optique comprennent la perte du champ visuel, la réduction de l’acuité visuelle, la dyschromatopsie, un défaut relatif de la pupille afférente (lorsqu’il est unilatéral ou asymétrique) et des lésions de la couche de fibres nerveuses rétiniennes. En l’absence d’une telle anomalie, vous devez vous demander si le patient présente une véritable atrophie optique.
La pâleur du disque optique, indiquant une atrophie optique, est plus une découverte qu’un diagnostic. Une fois identifié, une explication ou une cause sous-jacente doit être recherchée. Le terme pâleur ne doit jamais être utilisé de manière cavalière. Autrement dit, n’écrivez jamais que vous voyez ou soupçonnez une pâleur discale sur le dossier d’un patient, à moins qu’une enquête sur la cause ne soit entreprise. Si vous n’avez pas d’explication pour la pâleur discale, vous devez obtenir une neuroimagerie appropriée. Ne pas enquêter sur une découverte enregistrée de pâleur discale revient à écrire sur un dossier de patient: « Je pense que le patient peut avoir une tumeur au cerveau but mais je choisis de ne rien faire à ce sujet.”
Il existe de nombreuses causes d’atrophie optique, y compris la compression directe du nerf ou du chiasme par une lésion de masse, un infarctus, un traumatisme, une inflammation toxique, une infiltration et un dysfonctionnement métabolique, pour n’en nommer que quelques-unes.
Les lésions compressives Qui provoquent une pâleur discale
La neuropathie compressive par une lésion de masse peut souvent entraîner une pâleur discale et une atrophie optique. Une compression prolongée entraîne une atrophie optique, qui peut se manifester par une pâleur et / ou un bombement de la tête nerveuse. Des vaisseaux collatéraux optociliaires peuvent être notés à la marge du disque.2,3 Fréquemment, il y aura une augmentation progressive des ventouses de la tête du nerf optique, quelque peu similaire à celle observée dans le glaucome.4-6 Le principal facteur de différenciation de l’atrophie optique glaucomateuse est la pâleur du bord neurorétinien restant dans la neuropathie compressive.

3. Le même patient que ci-dessus avait un défaut de champ visuel bitemporal secondaire à une tumeur chiasmale.
En outre, il existe un compromis du bord neurorétinal plus important sous la forme d’entailles qui se produit dans le glaucome mais pas dans les lésions compressives, où l’augmentation de la cupule est plus symétrique avec la pâleur. Les défauts de champ associés aux lésions compressives comprennent les scotomes centraux, les défauts arqués ou altitudinaux, les scotomes paracentraux, la constriction du champ et les défauts respectant la ligne hémianopique verticale.
L’impact direct du nerf optique est le mécanisme de compromis dans la neuropathie optique compressive. Le plus souvent, cela provient d’une masse occupant l’espace dans l’orbite; bien qu’il puisse se produire au niveau du chiasme optique ou de la citerne suprasellaire. Dans ces cas, le patient aura probablement une perte de champ visuel orientée verticalement.
Les affections associées à la neuropathie optique compressive comprennent: une artère carotide dolichoectatique; une mucocèle; une ophtalmopathie thyroïdienne; des néoplasmes, y compris des gliomes du nerf optique, des méningiomes de la gaine nerveuse, des kystes dermoïdes, des neurilemmomes (schwannomes) et des métastases orbitales; des anomalies vasculaires, telles qu’un hémangiome caverneux, un lymphangiome, un varix veineux simple, une malformation artérioveineuse, un anévrisme carotidien et une fistule carotidienne caverneuse; inflammations, y compris cellulite orbitale et pseudotumeur orbital; granulomatose de Wegener; et hémorragie sous-périostée ou intraorbitale.7-16
La pathogenèse de cette condition est une compression mécanique du nerf qui induit une stagnation du flux axoplasmique dans les neurones individuels – dans les phases lentes et rapides du transport axoplasmique. Cette stase axoplasmique provoque un gonflement ultérieur des axones ainsi qu’une fuite de fluides intracellulaires, de lipides et de protéines dans l’espace extracellulaire du disque optique prélaminaire.
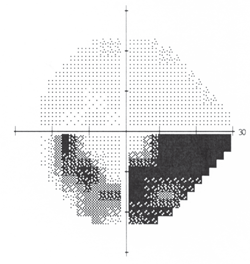
4. Défaut arqué inférieur compatible avec le glaucome.
Les changements vasculaires se produisent secondairement, car le drainage veineux via la veine rétinienne centrale est entravé par une contrainte mécanique continue. Comme ce processus persiste, l’hypoxie et la désorganisation de la matrice neurale normale s’ensuivent. Si elle n’est pas traitée, une atrophie optique s’ensuivra finalement. L’atrophie peut être totale ou sectorielle.
En 1998, David Greenfield, MD, et ses collègues ont publié un article fondateur discutant des patients atteints de glaucome qui ont besoin de neuroimagerie.17 Dans leur analyse rétrospective, ils ont comparé des patients atteints de glaucome présentant une pression intraoculaire normale (PIO) et ayant subi une neuroimagerie dans le cadre de leur évaluation (en raison de la PIO normale) avec des patients chez lesquels des lésions compressives ont été diagnostiquées.
Ils ont noté qu’aucun des patients diagnostiqués avec un glaucome à tension normale ne présentait de signes neuroradiologiques d’une lésion de masse dans la voie visuelle antérieure. Ils ont également constaté que, par rapport au groupe témoin présentant des lésions de masse, les patients atteints de glaucome étaient plus âgés et présentaient une meilleure acuité visuelle, une plus grande perte verticale du bord neurorétinal, des hémorragies discales plus fréquentes, moins de pâleur du bord neurorétinal et plus de défauts du faisceau de fibres nerveuses alignés le long de la ligne médiane horizontale.
En revanche, les patients présentant des lésions massives de la voie visuelle antérieure étaient généralement âgés de moins de 50 ans et présentaient une acuité visuelle inférieure à 20/40, des défauts de champ visuel alignés verticalement et une pâleur du disque optique dépassant les ventouses (figure 1). Ils ont conclu que le jeune âge, les niveaux d’acuité visuelle plus faibles, les défauts du champ visuel alignés verticalement et la pâleur du bord neurorétinien étaient plus indicatifs d’une lésion de masse compressive que le glaucome.
Exemples de cas
Cas 1. Un homme noir de 56 ans s’est présenté pour une consultation sur le glaucome. Il avait reçu un diagnostic de glaucome six ans plus tôt au Nigeria, mais n’avait jamais reçu de traitement.
Son acuité visuelle la mieux corrigée était de 20/30 O.D. et sa perception de la lumière O.S. Ses pupilles étaient égales et réactives avec un défaut afférent relatif gauche. La PIO était de 30 mm Hg O.D. et de 23 mm Hg O.S. La biomicroscopie n’a révélé aucune anomalie et la gonioscopie a démontré des angles de chambre antérieure normaux et ouverts.
L’examen du fond d’œil dilaté a révélé une coupe du disque optique de 0,75 /0,75 O.D. et de 0,80/ 0,80 O.S. Il y avait des dommages distincts au bord neurorétinien gauche. L’analyse de la couche de fibres nerveuses par polarimétrie laser à balayage était anormale dans l’œil gauche. Cependant, ce qui était le plus remarquable, c’était que le bord neurorétinien gauche restant était pâle par rapport à celui de l’œil de l’autre (figure 2).
Le patient présentait clairement une atrophie optique de l’œil gauche. De plus, son acuité de perception de la lumière n’était pas compatible avec un ventouses du disque optique de 0,80 / 0,80, si le glaucome en était la seule cause. À ce stade, on lui a diagnostiqué un glaucome comme une condition potentielle et on le soupçonne d’avoir également une neuropathie supplémentaire.
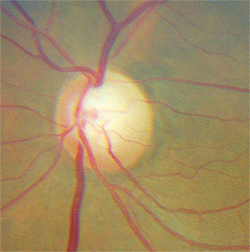
5. Le même patient que ci-dessus a démontré une entaille et une pâleur supérieures du bord.
La périmétrie de seuil a révélé un défaut de champ visuel bitemporal qui respectait la ligne hémianopique verticale de l’œil droit et se traversait pour impliquer une fixation dans l’œil gauche (figure 3). Cela correspondait à une tumeur du chiasme. L’imagerie par résonance magnétique (IRM) a confirmé le diagnostic.
Ce patient avait une tumeur ainsi qu’un glaucome. La principale constatation diagnostique était la pâleur discale et la perte d’acuité visuelle bien pire que ce à quoi on s’attendait d’un glaucome, ainsi que la perte de champ visuel orienté verticalement.
Cas 2. Une femme noire de 53 ans a été référée pour suspicion de glaucome. Elle n’avait aucune plainte visuelle ou oculaire. Son acuité visuelle la mieux corrigée était de 20/20 dans chaque œil.
Les pupilles étaient réactives, avec un défaut afférent relatif à l’œil gauche. Les tests de vision des couleurs étaient normaux. Il n’y avait pas d’anomalies biomicroscopiques et les angles de sa chambre antérieure étaient ouverts gonioscopiquement. La pression intraoculaire mesurée à 30 mm Hg O.D. et à 32 mm Hg O.S.
La périmétrie de seuil a révélé un champ O.D. plein et normal et un défaut arqué inférieur dense O.S., ce qui était compatible avec le glaucome (figure 4). L’examen dilaté a soulevé des inquiétudes. Son disque optique droit était rose, distinct et normal. Cependant, le nerf gauche du patient, tout en démontrant une entaille du bord neurorétinal temporal supérieur, était également pâle dans cette région (figure 5).
Bien que son acuité et sa vision des couleurs soient normales et que sa PIO se situe clairement dans une plage glaucomateuse, l’unilatéralité et la présence d’une pâleur discale dans son œil gauche ont soulevé la suspicion d’une tumeur compressive du nerf optique. Le patient a subi une IRM des orbites et du chiasme — avec et sans contraste – qui s’est avérée normale.
Malgré l’apparence suspecte du disque, le patient n’a rien de plus qu’un glaucome et continue de bien fonctionner avec le traitement topique du glaucome.
Considérez Les Causes rétiniennes
Cas 3. Un Indien de 72 ans a été référé pour une consultation sur le glaucome. Il était depuis longtemps suspecté d’un glaucome à tension normale dû à une forme légèrement asymétrique de ventouses discales et à une perte de champ visuel observée plusieurs années plus tôt.
Il avait été vu par un certain nombre de médecins dans un cadre universitaire. Il avait reçu un traitement au glaucome par intermittence, et son dossier a révélé qu’aucun essai médicamenteux n’avait jamais semblé abaisser sa PIO en dessous de sa plage non traitée de 12 mm Hg à 14 mm Hg.
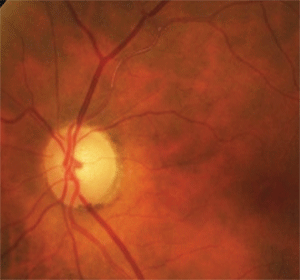
6. La pâleur discale temporale supérieure et l’artériole sclérosée et occlusive étaient dues à une ancienne occlusion asymptomatique de l’artère rétinienne branchiale.
Ses antécédents médicaux étaient significatifs pour une hypertension contrôlée et une hypercholestérolémie. Après avoir examiné les antécédents du patient et un traitement médical apparemment inefficace, un médecin précédent a suggéré de surveiller le patient sans traitement. Plus récemment, un autre médecin de l’établissement avait noté une pâleur discale supérieure dans l’œil gauche et avait demandé un autre avis.
L’acuité visuelle la mieux corrigée du patient était de 20/20 O.D. et O.S. Il n’y avait aucun défaut pupillaire afférent relatif dans les deux yeux. Le patient n’avait aucune plainte visuelle ou oculaire, mais comprenait qu’il était suspect de glaucome en raison de ce qui lui avait été expliqué au cours des dernières années.
L’analyse de la périmétrie du seuil passé a révélé un scotome arqué inférieur immuable dans l’œil gauche et un champ visuel normal dans l’œil droit. L’inspection du fond d’œil dilaté des nerfs optiques a révélé un rapport coupe-disque de 0,6 x 0,5 U. Le disque optique droit était normal sans pâleur ni changements glaucomateux. Il n’y avait pas de compromis focal du bord neurorétinien de l’œil gauche, ce qui expliquerait la perte de champ visuel si le glaucome en était la cause. Cependant, il y avait une pâleur du disque supérieur de l’œil gauche, ce qui correspondait à la perte de champ. Ainsi, le patient présentait une pâleur discale dépassant les ventouses, indiquant une cause autre que le glaucome.
À cette fin, une inspection minutieuse du système vasculaire rétinien adjacent a révélé une sclérose de l’artériole temporale supérieure avant et au-delà de la première bifurcation (figure 6). De plus, il y avait de faibles vaisseaux collatéraux rétiniens dans la région temporale supérieure qui indiquaient une occlusion vasculaire rétinienne antérieure. Dans ce cas, la perte de champ et la pâleur discale du patient étaient dues à une ancienne occlusion asymptomatique de l’artère rétinienne de la branche.
Approche de la pâleur discale
Lorsque la pâleur discale optique est observée, cherchez à corroborer la découverte d’un dysfonctionnement du nerf optique. Assurez-vous d’effectuer des tests de vision des couleurs, une inspection des pupilles, une périmétrie de seuil, une mesure de l’acuité visuelle la mieux corrigée et une évaluation de la couche de fibres nerveuses rétiniennes. Ces tests peuvent vous guider vers l’emplacement et la nature du problème.
Les antécédents du patient sont cruciaux. Vérifiez si le patient est au courant de tout changement. En cas de perte de vision, essayez de déterminer si la réduction était progressive (indicative de lésions compressives) ou brutale (suggérant un infarctus du nerf optique ou de la rétine). Identifiez s’il y avait une douleur associée à une perte de vision (comme celle observée dans la névrite optique) ou si la condition était indolore (compatible avec une neuropathie optique ischémique antérieure non artéritique). Enfin, examinez attentivement les antécédents médicaux passés et présents du patient pour détecter toute condition contributive possible, telle que la sclérose en plaques, la dysfonction thyroïdienne ou le cancer.
Si une compression du nerf optique est suspectée, une IRM des orbites et du chiasme, avec et sans contraste, doit être ordonnée. De préférence, cette imagerie doit être réalisée dans une unité fermée, car les détails seront meilleurs. Lorsque la compression de la voie visuelle chiasmale ou antérieure est suspectée, l’imagerie des orbites et du chiasme sera plus révélatrice que celle du cerveau.
Gardez à l’esprit que la pâleur du disque optique est plus une découverte qu’un diagnostic et qu’une cause doit être recherchée. Ne jamais enregistrer la pâleur discale dans le dossier d’un patient sans d’abord expliquer ou agir sur cette constatation. Différencier soigneusement la pâleur discale de l’atrophie glaucomateuse.
Rappelez-vous toujours que la pâleur en excès de ventouses indique autre chose que — ou en plus du glaucome, mais que rien n’entaille un nerf comme le glaucome.
Le Dr Sowka est professeur au Nova Southeastern University College of Optometry à Fort Lauderdale, en Floride. Il est également Chef des Soins avancés et Directeur des Services de glaucome à l’Institut de soins oculaires de l’Université Nova Southeastern.
1. Snydacker D : Le disque optique normal. Études ophtalmoscopiques et photographiques. Am J Ophthalmol 1964; 58:958-964. Wilhelm H, Dörr S, Paulsen F, et al. Premiers symptômes et découvertes dans les méningiomes du nerf optique. Klin Monbl Augenheilkd. 2009 Nov; 226 (11): 869-74.
3. Rebolleda G, Corcóstegui J, Arruabarrena C, et al. Vaisseaux de dérivation optociliaires dans la neuropathie optique compressive par l’artère carotide interne intracrânienne. Eur J Ophthalmol. 2008 Mars-avril; 18 (2): 316-9.
4. Roodhooft JM. Nonglaucomatous optic disk atrophy and excavation in the elderly. Bull Soc Belge Ophtalmol. 2003;(287):45-9.5. Hokazono K, Moura FC, Monteiro ML. 5. Optic nerve meningioma mimicking progression of glaucomatous axonal damage: a case report. Arq Bras Oftalmol. 2008 Sep-Oct;71(5):725-8.
6. Greenfield DS. Glaucomatous versus nonglaucomatous optic disc cupping: clinical differentiation. Semin Ophthalmol. 1999 Jun;14(2):95-108.
7. Rosen N, Ben Simon GJ. Orbital decompression in thyroid related orbitopathy. Pediatr Endocrinol Rev. 2010 Mar;7(Suppl 2):217-21.
8. Mlle, McNab AA. Décompression orbitale dans l’orbitopathie de Graves: efficacité et sécurité. Stagiaire Med J. 2005 Oct; 35 (10): 586-91.
9. Robert PY, Camezind P, Adenis JP. Complications de l’ophtalmopathie dysthyroïdienne. J Fr Ophtalmol. 2004 Sep; 27(7): 819-21.
10. Oono S, Kurimoto T, Fukazawa K, Mimura O. Neuropathie optique compressive causée par un kyste sinusal paranasal de la granulomatose de Wegener. Jpn J Ophthalmol. 2007 Nov-Déc; 51(6): 480-1.
11. Chua CN, Alhady M, Ngo CT, et al. Neurofibrome nasal solitaire se présentant comme une neuropathie optique compressive. Oeil (Lond). 2006 Déc; 20 (12): 1406-8.
12. Mansour AM, SALUT Salti. Myélome multiple présentant une compression du nerf optique. Oeil (Lond). 2001 Déc; 15 (Pt 6): 802-4.
13. Wu W, Sun MT, Cannon PS, et al. Récupération de la fonction visuelle chez un patient atteint d’une neuropathie optique compressive à la mucocèle à cellules onodi qui avait un intervalle de 5 semaines entre le début et l’intervention chirurgicale: un rapport de cas. J Ophthalmol. 2010;2010:483056. Epub 2010 12 octobre.
14. George JL, Marchal JC. Tumeurs orbitales chez l’enfant: examen clinique, imagerie, progression spécifique. Neurochirurgie. 2010 Avril-juin; 56 (2-3): 244-8.
15. Aakalu VK, Ahmad AZ. Granulomatose de Wegener provoquant une neuropathie optique compressive chez un enfant. Ophthal Plast Reconstr Surg. 2009 Juil-août; 25 (4):327-8.
16. Jacobson DM. Compression symptomatique du nerf optique par l’artère carotide: profil clinique de 18 patients avec 24 yeux affectés identifiés par imagerie par résonance magnétique. Ophtalmologie. 1999 Oct; 106 (10): 1994-2004.
17. Greenfield DS, Siatkowski RM, Glaser JS, et al. Le disque en coupe: Qui a besoin de neuroimagerie? Ophtalmologie. 1998 Oct; 105:1866-74.
Leave a Reply