Organes imprimés en 3D À l’approche des essais cliniques
À l’aide de l’impression 3D et de l’électrospinning, une équipe de bioingénieurs du Wake Forest Institute for Regenerative Medicine dirigée par Anthony Atala développe des tissus et des organes viables pour les patients. Bien que bon nombre de ces organes imprimés en 3D restent au stade de la recherche, certains devraient être prêts pour des tests cliniques d’ici un an ou deux.
Depuis plus de 25 ans, Atala travaille sur la génération de cellules tissulaires en laboratoire. Des doigts et des oreilles aux reins et aux cœurs, son équipe peut désormais créer 40 structures d’organes et de tissus différentes.
Qu’Est-Ce Que L’Électrofinçage ?
Ces procédures commencent par prélever un petit échantillon des cellules du patient dans la zone que les bioingénieurs tentent de recréer. Par exemple, pour la peau, ils n’ont besoin que d’une greffe à peu près aussi grande qu’un timbre-poste. Ensuite, dans un bioréacteur, ils répliquent ces cellules jusqu’à ce qu’il y en ait assez pour faire pousser l’organe.
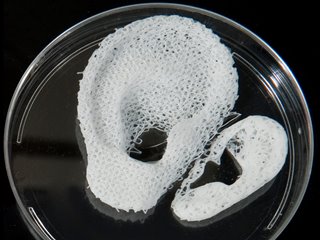 Les bioprinters 3D déposent différents types de cellules de la même manière qu’une imprimante 3D couleur dépose différents types de polymères. Photo: Wake Forest
Les bioprinters 3D déposent différents types de cellules de la même manière qu’une imprimante 3D couleur dépose différents types de polymères. Photo: Wake ForestL’étape suivante consiste à construire la matrice extracellulaire, ou échafaudage, sur laquelle se forment les cellules. L’équipe ensemence ensuite la matrice avec des promoteurs de croissance et des produits biochimiques qui incitent les cellules à se développer de manière spécifique. La matrice fournit également des forces mécaniques qui façonnent le développement cellulaire.
Pour fabriquer des structures, comme la peau ou les vaisseaux sanguins, le laboratoire utilise l’électrospinning, une technique d’impression 3D qui ressemble aux machines utilisées pour transformer le sucre en barbe à papa.
Les bioingénieurs utilisent cette technique pour faire tourner un polymère hydrogel à grande vitesse, forçant le polymère à s’allonger en longs brins de fibres. Ils placent ensuite une fine tige au centre de la machine. Les fibres d’hydrogel adhèrent à la tige tout comme la barbe à papa moelleuse se fixe à un cône en papier. Les scientifiques manipulent la forme du polymère spongieux en faisant varier la tension jusqu’à ce qu’ils aient imité la structure qu’ils créent.
Pour en savoir plus: Impression 3D de la peau vivante avec des vaisseaux sanguins
Une fois que les chercheurs ont atteint la forme désirée, ils pulvérisent les cellules du bioréacteur sur la matrice, la superposant de manière répétitive pour correspondre aux structures naturelles. Pour recréer la peau, par exemple, ils commenceraient par appliquer des cellules de la couche sous-cutanée puis celles du derme et de l’épiderme.
Une fois posée sur la matrice, la structure est placée dans un incubateur qui imite les conditions du corps humain. Là, cette combinaison de matrice, de produits biochimiques et de cellules commence à prendre une vie propre, en utilisant la matrice comme guide.
Bien que cette technique soit parfaite pour les structures simples et légères, comme la peau et les vaisseaux sanguins, elle n’a pas la précision et la capacité de créer des structures tridimensionnelles solides comme un cœur.
Comment imprimer des Organes solides?
Pour créer un organe solide, les chercheurs ont besoin d’un moyen de favoriser la croissance des vaisseaux sanguins afin que chaque cellule de l’organe reçoive l’oxygène et les nutriments et puisse éliminer les déchets. La création de ces arbres de vaisseaux sanguins, qui se ramifient des grandes artères aux plus petits vaisseaux, a perplexe les chercheurs pendant des décennies. Pourtant, l’équipe d’Atala a développé quelques solutions potentielles.
 Une des nombreuses imprimantes 3D conçues pour imprimer des cellules. Photo: Wake Forest
Une des nombreuses imprimantes 3D conçues pour imprimer des cellules. Photo: Wake ForestLa première solution commence par un organe donneur existant, tel qu’un foie. Tout d’abord, les bioingénieurs de Wake Forest le placent dans un shaker, un peu comme une machine à laver, avec des détergents doux pendant environ deux semaines.
« Après avoir traversé le shaker, vous pouviez tenir l’organe et il ressemblerait à l’organe, mais il n’aurait pas de cellules”, a déclaré Atala. » Essentiellement, nous avions conservé le squelette de l’orgue. »
Ce squelette est constitué de collagène, une protéine présente dans le tissu conjonctif de l’organisme et ses matrices extracellulaires. Comme la matrice électropompe, la matrice de collagène fournit la structure et les forces mécaniques dont les cellules ont besoin pour se diviser et assumer des fonctions liées aux organes. Le squelette de l’organe est ensuite déposé dans les cellules hépatiques du patient, qui repeuplent l’organe, le ramenant à la vie avec de nombreuses fonctions d’un foie humain.
Bien que cette méthode soit prometteuse, elle signifie toujours attendre un organe donneur avec lequel travailler. L’impression 3D peut offrir un moyen de contourner cela. Cette méthode prend beaucoup plus de compréhension de l’organe lui-même, mais promet de libérer les patients de l’attente d’un organe donneur.
Pour en savoir plus: La Bioprinter 3D Imprime une Peau saine sur les Patients en quelques minutes
« Il se passe tellement de choses dans un organe comme le cœur que nous ne pouvons pas voir si nous ne partons pas de zéro”, a déclaré Atala. « Nous examinons la structure d’un point de vue à 360 degrés pour nous assurer que nous pouvons reproduire la fonctionnalité de l’orgue de toutes les manières possibles, sinon il ne survivra pas. »
Une façon de le faire est de continuer à construire des organes et d’apprendre des constructions. À cette fin, Atala et son équipe ont conçu plus d’une douzaine d’imprimantes pour réaliser les processus complexes de construction d’un orgue solide. Les imprimantes fonctionnent comme des imprimantes à jet d’encre couleur, mais au lieu de l’encre, leurs cartouches contiennent des cellules séparées par type.
Pour commencer, la bioprinter est chargée d’informations sur les patients et les organes, un plan de ce qu’il faut construire. Grâce à un système de buses, l’imprimante dépose des couches de cellules sous forme de gel épais. Cela génère lentement la structure de l’organe tout en préservant la vie des cellules qui y sont intégrées.
Alors que l’équipe maîtrise encore cette forme d’ingénierie topographique, l’impression 3D permet aux chercheurs de travailler les détails. Par essais et erreurs, ils ont réussi à programmer les imprimantes pour déposer même les plus petits vaisseaux sanguins dans un organe complexe.
La bio-impression 3D est-elle l’avenir de la transplantation d’organes?
Quelle que soit la technique utilisée par l’équipe, il faut environ quatre à six semaines pour construire un remplaçant sain pour un patient. Étant donné que le tissu ou l’organe de remplacement est fabriqué à partir des propres cellules du patient, il n’y a pratiquement aucune probabilité de rejet — ce qui signifie que les patients guérissent plus rapidement que jamais et n’ont pas besoin de prendre de médicaments pour empêcher leur système immunitaire d’attaquer la greffe.
Pour en savoir plus: Top 10 des tendances de la bioingénierie pour 2020
« Pouvoir créer ces structures avec les propres cellules d’un patient où elles peuvent vraiment s’adapter et guérir, c’est l’espoir pour nous”, a déclaré Atala. « Nous voulons nous assurer que nous pouvons atteindre le plus de patients possible. »
Atala dit que les structures plus simplifiées comme la peau et les vaisseaux sanguins ont déjà eu des essais humains réussis et seront en clinique dans quelques années. Les organes solides prendront beaucoup plus de temps.
Cela a été un voyage remarquable pour Atala et ses progrès ont jeté les bases et la base de connaissances pour une génération réussie de tissus cellulaires humains.
Cassie Kelly est une rédactrice en ingénierie et en environnement basée à Columbus, Ohio.
Inscrivez-vous aujourd’hui à AM Medical: 27-28 mai 2020 à Minneapolis, MN
Leave a Reply