7.2:범용성
소개
범용성은 하나의 가장 효소를 공부하로 인해 두 가지 단계 속도:pre-steady-state 고 꾸준 상태입니다. 연구의 이러한 두 가지 운동국을 제공합의 증거로”탁구”메커니즘의 형성,공유지를 선도하는 공유결합 분해 반응의 속도 촉매 반응이다. 키모 트립신의 합성은 주로 췌장에서 발생합니다. 그러나 활성 형태 대신에 chymotrypsinogen 이라고 불리는 비활성 zymogen 으로 생산되어 프로테아제 활성이 췌장을 소화하지 못하게합니다. 소장의 내강으로 분비되면 트립신이라는 또 다른 효소에 의해 활성 형태로 전환됩니다. 이존의 다른 효소의 활성화를 위해 프로테아제는 일반적인 방법으로 방지하기 위해 몸의 소화 기관 및 기타 유해 효소 부작용이 나타납니다.
범용성을 통해 운영하는 일반적인 메커니즘은 알려져 있으로 탁구 메커니즘(그림\(\PageIndex{1}\))그것에 의하여 효소 반응으로 기판을 형성하는 효소이다. 이 중간체는 초기 효소와 다른 성질을 가지므로 초기 효소 활성을 재생하기 위해서는 2 차 기질과 반응해야합니다. 이 프로세스는 다음과 같습니다.
더 구체적으로,범용성을 운영하고 특정 유형의 탁구라는 메커니즘을 공유 결합을 가수분해. 이것은 효소가 먼저 표적 기질과 공유 결합을 형성하여보다 안정한 모이어 티를 용액으로 변위시키는 것을 의미합니다. 이 효소-기질 복합체를 효소 중간체라고합니다. 그런 다음 중간체는 물 과 반응하여 초기 기질의 나머지 부분을 변위시키고 초기 효소를 개질합니다.
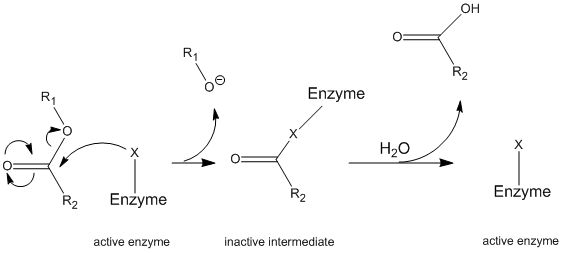
키모 트립신은 대부분의 효소와 마찬가지로 반응하는 기질의 유형에 특이 적입니다. 프로테아제로서,폴리 펩타이드를 절단하고,그 고유 한 특이성은 방향족 잔기의 카르복시 말단에서만 작용할 수있게한다. 그것은 다소 복잡한 메커니즘이며 일련의 단계에서 가장 잘 설명됩니다.
1. 대상을 입력 active 사이트의 범용성,그리고 그가 거기 개 소수에 의해 간의 상호 작용 노출된 비극의 그룹 효소 및 잔류물 비극 방향족 사이드 체인의 기판이다. 히스티딘-57 의 쉬프 질소와 세린-195 의 산소 측쇄 사이의 수소 결합에 주목하는 것이 중요합니다.
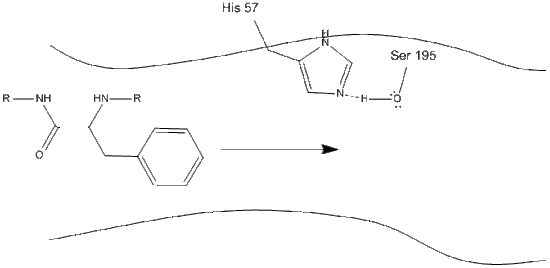
2. 도움히스티딘-떠들고 수소결합,수산기 그룹에서 떠들고 195 수행 닐 공격에서 카르보닐 탄소의 방향족 아미노산과 동시에 전송 수산화 수소를히스티딘 쉬프 질소입니다. 이 공격은 밀어 pi 전자 카르보닐기에 카르보닐기의 산소를 형성,수명이 짧은 중간으로 구성된 c-terminal 탄소 네 단일채: 산소 음이온,방향족 아미노산의 베타-탄소,기질 단백질의 후속 아미노산의 n-말단,및 세린-195 측쇄 산소.나는 이것이 내가 할 수있는 유일한 방법이라고 생각한다.gif
3. 이 중간체는 oxyanion 전자가 방향족 아미노산의 c 말단과 pi 결합을 개질함에 따라 수명이 짧습니다. 유대 사 carboxy terminus 의 방향족 아미노산,n-말단 이후의 잔류물은 흘리며,전자가 추출하는 데 사용되는 수소의 protonated 쉬프 질소에서히스티딘-57. 카르 보닐 탄소와 세린 -195 산소 사이의 결합은 에스테르 구성으로 유지됩니다. 이것을 아실-효소 중간체라고합니다. 폴리펩티드의 c 말단 측은 이제 효소의 활성 부위로부터 해리되어 자유 롭다.
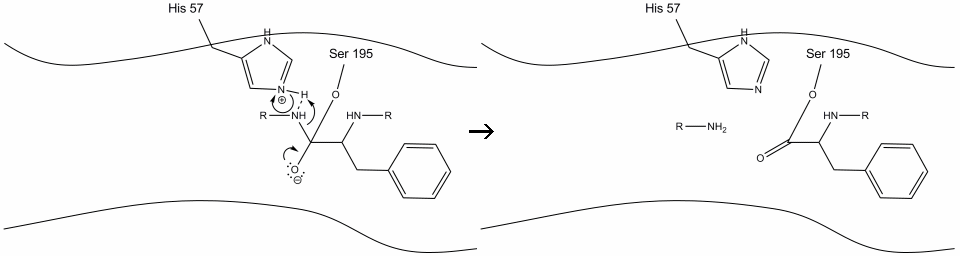
4. 물 분자는 이제 물 수소 원자와 히스티딘-57 쉬프 질소 사이의 수소 결합을 통해 활성 부위에 들어가고 결합 할 수 있습니다.
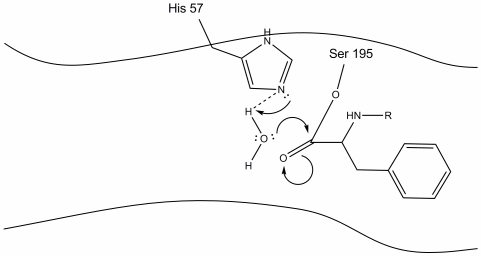
5. 의 물 산소 지금 닐 공격에서 카르보닐기의 탄소 acyl-효소 중급,추진 카르보닐기의 파이 전자에 카르보닐로 탄소히스티딘-57 추출물 양자 중 하나에서 물. 이것은 세린,수산기,옥시 아니온 및 방향족 아미노산과 공유 결합 된 또 다른 4 차 탄소를 형성한다. 최근에 양성자 화 된 히스티딘-57 의 양성자는 이제 세린 산소와 수소 결합을 만들 수 있습니다.
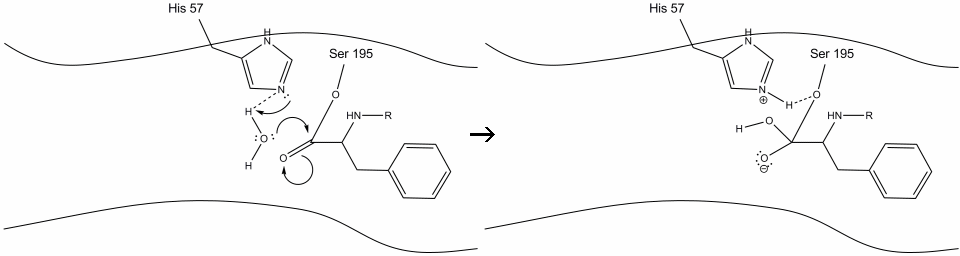
6. 옥시 아니온 전자는 카르 보닐 파이 결합을 개질하여 카르 보닐 탄소와 세린 히드 록실 사이의 결합을 절단한다. 이 결합의 전자는 히스티딘 쉬프 질소를 탈 프로토 네이트하고 원래의 효소를 개질하기 위해 세린 산소에 의해 사용된다. 기판은 더 이상 활성 부위에 대한 친 화성을 갖지 않으며,곧 복합체로부터 해리된다.
Leave a Reply