Știri-leucemie congenitală după abuz greu de spray permetrin în timpul sarcinii

raport de caz
leucemie congenitală după abuz greu de spray permetrin în timpul sarcinii
a Borkhardt, m Wilda, U Fuchs, l Gortner și i Reiss
Spitalul Universitar pentru copii Giessen, Feulgenstr 12, 35392 Giessen, Germania
corespondență cu:
Dr.Borkhardt, hematologie pediatrică și oncologie, feulgenstr 12, 35392 Giessen, Germania;
Arndt.borkhardt {at}pediatru.med.uni-giessen.de
acceptat 6 octombrie 2002
rezumat
este descris un singur caz de leucemie congenitală cu rearanjare 11q23 / MLL la un nou-născut prematur. Din cauza arahnofobiei, mama a abuzat puternic de permetrin aerosolizat, un insecticid de uz casnic utilizat pe scară largă. Permetrinul este considerat relativ sigur, dar, având în vedere istoricul mamei, a fost testat potențialul său de a induce scindarea genei MLL în cultura celulară. Incubarea liniei celulare BV173 cu un permetrin de 50 de centimetri indus ușor de clivajul MLL.
cuvinte cheie: leucemie congenitală; leucemie; permetrin; insecticid; 11q23/MLL
leucemia congenitală este o boală rară care afectează aproximativ un copil din 200 000-250 000 de nașteri vii pe an. În ciuda rarității sale, leucemia congenitală a stimulat mult interes din cauza oportunității de a afla mai multe despre cauzele care stau la baza leucemogenezei in utero. Există mulți factori de risc care pot crește șansa inducerii precoce a unui fenotip leucemic—de exemplu, expunerea părinților la toxine profesionale și de mediu, utilizarea tutunului, marijuanei, alcoolului și a altor toxine.1 leucemia congenitală și infantilă sunt adesea asociate cu rearanjări ale genei MLL la cromozomul 11q23.2 Mai multe substanțe au fost examinate pentru potențialul lor de a traversa bariera placentară și de a induce o astfel de Ruptură cromozomială la 11q23/MLL.3,4
aici extindem lista medicamentelor capabile să scindeze gena MLL, cel puțin atunci când celulele sunt expuse în cultură. Împreună cu un istoric de caz destul de neobișnuit, datele noastre experimentale aruncă o lumină asupra generării leucemiei congenitale și pot ajuta la prevenirea unora dintre cazurile fatale ale acestei boli.
raport de caz
O femeie sănătoasă de 27 de ani a fost internată la secția de ginecologie din cauza travaliului prematur. Era în a 35-a săptămână de la prima sarcină. Controalele prenatale au fost normale. Deoarece cardiotocograma nu a arătat ritm cardiac fetal, a fost planificată o operație cezariană de urgență. Cu toate acestea, șase minute mai târziu, femeia a născut spontan un copil prematur care cântărea 2300 g și nu prezenta semne vitale, ci o culoare lividă izbitoare a pielii. Resuscitarea cardiopulmonară primară a fost începută imediat cu intubație endotraheală, compresie toracică și administrare repetată de adrenalină. Cu toate acestea, scorul Apgar a rămas 0 după cinci și 10 minute. Echipa de urgență pediatrică a sosit 10 minute mai târziu și a continuat să efectueze resuscitare cardiopulmonară. O linie centrală a fost realizată prin cateterizarea venei ombilicale. La 25 de minute după partum, a fost stabilită o circulație stabilă, cu o frecvență cardiacă de 140 bătăi/min. Un examen fizic a arătat hepatomegalie de 5 cm sub marginea costală și infiltrații nodulare livide ale pielii (fig.1a de mai jos).
|
|
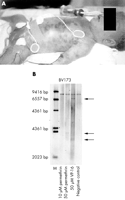
figura 1 (A) pacientul la vârsta de 2 ore. Rețineți infiltrarea leucemică a pielii („pete de afine”). (B) Southern blot care prezintă o rearanjare MLL în linia celulară BV173 incubată cu permetrin de 50 de centimetri timp de șase ore. Clivajul MLL indus de VP16 a fost utilizat ca control. |
în afară de anatomia normală a inimii, ecografia a arătat hipertensiune pulmonară substanțială combinată cu insuficiență de gradul doi până la trei al valvei tricuspide. Pe lângă hepatomegalie, a fost găsită o hemoragie intracraniană bilaterală. Pentru o oxigenare suficientă și îndepărtarea dioxidului de carbon, a fost necesară ventilația de înaltă frecvență cu 10 Hz, FIO2 = 1 și o presiune medie a căilor respiratorii de 13 cm H2O. numărul inițial de celule albe din sânge a fost de 400 000/unktil cu un exces de celule blastice mieloide. Examinarea măduvei osoase a confirmat diagnosticul de leucemie mieloidă acută congenitală, cu 95% celule blastice de morfologie mielomonocitară (FAB-M5). A fost efectuat un schimb complet de sânge, care a redus numărul de celule albe din sânge la 56 000/unktil și a dus la o îmbunătățire a oxigenării și ventilației. Douăsprezece ore mai târziu, numărul de celule albe din sânge a crescut din nou, la 125 000/unktil. Oxigenarea membranei extracorporale a fost luată în considerare, dar în cele din urmă respinsă din cauza hemoragiei intracraniene progresive care implică o suprafață mare a parenchimului. Copilul a murit la 48 de ore după naștere din cauza eșecului multiorgan. În afară de leziunile cerebrale severe deja diagnosticate prin ultrasunete, autopsia a arătat infiltrarea difuză a plămânilor, ficatului, splinei și cutisului.
experimente pe culturi celulare: inducerea rearanjamentelor MLL de către permetrin
Testul experimental a fost efectuat exact așa cum este descris de Strick și colab., 3 care au analizat o gamă largă de substanțe naturale din alimente și suplimente alimentare pentru capacitatea lor de a induce clivajul specific site-ului în cadrul genei MLL.
rezultate și discuții
analiza citogenetică a aspiratului măduvei osoase a arătat prezența unei translocații t(11;19)(q23;p13) în toate metafazele analizate. Mai mult, am arătat o rearanjare a oncogenei MLL la cromozomul 11q23 prin sugativă sudică. Imunofenotiparea de rutină a arătat expresia CD15, CD33, CD 65s și MPO (datele nu sunt afișate). În studiile anterioare, anticorpul monoclonal 7.1 a apărut ca un instrument imunofenotipic valoros pentru detectarea celulelor leucemice, cu expresia antigenului NG2 care se corelează puternic cu rearanjările MLL la sugari.5,6 în cazul nostru, totuși, colorarea cu acest anticorp monoclonal a rămas negativă, ceea ce ne-a împiedicat să efectuăm alte experimente de sortare a celulelor.
mama suferise aparent de arahnofobie încă din copilărie. Cu doi ani înainte de sarcină, a început să utilizeze în exces permetrinul aerosolizat. De atunci, ea a trăit singură. Oamenii au evitat să o viziteze din cauza mirosului pătrunzător din casa ei. Permetrinul este un insecticid de uz casnic utilizat pe scară largă, care oferă protecție împotriva vectorului malariei Anopheles.7,8 este, de asemenea, cunoscut a fi un medicament eficace împotriva scabiei și a capului păduchi pediculoză capitis.9,10 în comparație cu alte medicamente, este considerat sigur și utilizarea sa topică este recomandată chiar și pentru nou-născuții cu scabie.11 Cu toate acestea, a fost legată de generarea atât a aberațiilor cromozomiale în celulele măduvei osoase ale șoarecilor, cât și a leziunilor ADN în limfocitele umane.12-14 prin urmare, am emis ipoteza că permetrinul a traversat placenta femeii însărcinate și a afectat celulele precursoare hematopoietice din fătul în curs de dezvoltare, rezultând leucemogeneză. Prin urmare, am încercat să generăm rearanjările în oncogena MLL in vitro prin expunerea celulelor BV173 la permetrin de 50 de centimetri. După 24 de ore de expunere, celulele bv173 tratate cu permetrin au prezentat o rearanjare MLL clară, în timp ce celulele netratate au prezentat numai gena MLL de tip sălbatic (fig.1B de mai sus). Prin urmare, recomandăm cu tărie o mare precauție în utilizarea permetrinului în timpul sarcinii. Chiar dacă concluziile definitive nu pot fi trase dintr-un singur caz izolat, datele noastre sugerează cu tărie că permetrinul poate avea efecte secundare severe atunci când celulele precursoare hematopoietice fetale sunt expuse in utero. În același sens, un raport recent al unei colaborări multinaționale a indicat faptul că utilizarea medicamentelor împotriva țânțarilor în timpul sarcinii este asociată în mod semnificativ cu leucemia infantilă.4 este deosebit de demn de remarcat faptul că autorii au găsit această asociere numai pentru cazurile MLL rearanjate și nu pentru cazurile MLL germline. Acest lucru argumentează puternic împotriva prejudecății de selecție în studiul lor de caz-control și susține ipoteza că expunerea in utero provoacă rearanjările MLL.
în cele din urmă, mama în cazul nostru a fost tratată cu succes pentru arahnofobie prin psihoterapie. Doi ani mai târziu, ea a născut un băiat sănătos care nu avea semne clinice de leucemie și care este încă sănătos la vârsta de 13 luni.
mulțumiri
asistență tehnică Expert de Claudia Keller și Stefanie Garkisch este recunoscut cu recunoștință. Îi mulțumim lui Jochen Harbott, Giessen, Germania pentru că ne-a furnizat datele citogenetice. Datele imunofenotipice au fost furnizate cu amabilitate de către W-D Ludwig, Centrul de Cancer Robert R Inktssle, Universitatea Humboldt, Berlin, Germania. Studiile moleculare au fost susținute de Fundația Germană pentru Cancer (grant 10-1658-Bo2).
- Sande JE, Arceci RJ, Lampkin BC. Leucemie congenitală și neonatală. Semin Perinatol 1999; 23: 274-85.
- Ford AM, Ridge SA, Cabrera ME și colab. Rearanjări in utero în oncogena legată de trithorax în leucemiile infantile. Natură 1993; 363:358–60.
- Strick R, Strissel PL, Borgers S, și colab. Bioflavonoidele dietetice induc scindarea genei MLL și pot contribui la leucemia infantilă. Proc Natl Acad Sci SUA 2000;97:4790-5.
- Alexander FE, Patheal SL, Biondi A, și colab. Expunerea chimică transplacentară și riscul de leucemie infantilă cu fuziunea genei MLL. Cancer Res 2001; 61: 2542-6.
- Smith FO, Rauch C, Williams de, și colab. Omologul uman al șobolanului NG2, un proteoglican sulfat de condroitină, nu este exprimat pe suprafața celulară a celulelor hematopoietice normale, ci este exprimat prin explozii acute de leucemie mieloidă de la pacienții cu prognostic slab cu anomalii ale benzii cromozomiale 11q23. Sânge 1996; 87:1123-33.
- Behm FG, Smith FO, Raimondi SC și colab. Omolog uman al proteoglicanului sulfat de condroitină de șobolan, NG2, detectat de anticorpul monoclonal 7.1, identifică leucemiile limfoblastice acute din copilărie cu T(4;11) (q21;q23) sau t (11;19) (q23; p13) și rearanjările genei MLL. Sânge 1996; 87: 1134-9.
- Rowland M, Durrani N, Hewitt S, și colab. Chaddars și top-sheets tratate cu permetrin: tehnologie adecvată pentru protecția împotriva malariei în Afganistan și alte situații de urgență complexe. Trans R Soc Trop Med Hyg 1999; 93: 465-72.
- Binka FN, Mensah OA, Mills A. rentabilitatea setcilor de pat impregnate cu permetrin în prevenirea mortalității infantile în districtul Kassena-Nankana din nordul Ghanei. Politica De Sănătate 1997; 41:229-39.
- Blanshard ME, Schofield J. scabie: o abordare practică. Prof Îngrijire Mama Copil 1999; 9: 15-16.
- Dodd CS. Intervenții pentru tratarea capului. Cochrane baza de date Syst Rev 2000; CD001165.
- Quarterman MJ, Lesher JL, Jr. scabie neonatală tratată cu cremă de permetrină 5%. Pediatr Dermatol 1994; 11: 264-6.
- Cantalamessa F. toxicitatea acută a două piretroide, permetrin și cipermetrin la șobolanii neonatali și adulți. Arch Toxicol 1993; 67: 510-13.
- Barrueco C, Herrera A, Caballo C, și colab. Inducerea aberațiilor cromozomiale structurale în culturile limfocitelor umane și celulele CHO prin permetrină. Teratog Carcinog Mutagen 1994; 14: 31-8.
- Santoni G, Cantalamessa F, Spreghini E, și colab. Modificări ale distribuției și funcțiilor celulelor T la șobolanii expuși la cipermetrin prenatal: posibila implicare a catecolaminelor. Toxicologie 1999; 138: 175-87.
Leave a Reply