Szerves Kémia II

kísérletileg azonban megfigyelhető, hogy a C2-C3 kötés forgásának jelentős akadálya van, és hogy az egész molekula sík. Ezenkívül a C2-C3 kötés 148 pm hosszú, rövidebb, mint egy tipikus szén-szén egyetlen kötés (körülbelül 154 pm), bár hosszabb, mint egy tipikus kettős kötés (körülbelül 134 pm).
A molekuláris orbitális elmélet ezeket a megfigyeléseket a delokalizált pi kötések fogalmával magyarázza. Ebben a képen a négy 2P atompálya matematikailag kombinálódik, hogy négy pi molekuláris pályát képezzen a növekvő energia számára. Ezek közül kettő – a kötés pi orbitals-alacsonyabb energiájú, mint a P atomi orbitálok, amelyekből kialakulnak,míg kettő – az antibonding pi* orbitals-energiában magasabb.

a legkisebb energiájú molekulapályának, a pi1-nek csak konstruktív kölcsönhatása és nulla csomópontja van. Az energiában magasabb, de még mindig alacsonyabb, mint az izolált p orbitálok, a pi2 orbitálnak egy csomópontja van, de két konstruktív kölcsönhatása van – tehát ez még mindig egy kötés orbitális. A két antibonding orbitálra nézve a pi3* – nak két csomópontja és egy konstruktív kölcsönhatása van, míg a pi4 * – nak három csomópontja és nulla konstruktív kölcsönhatása van.
az Aufbau-elv alapján az izolált 2PZ atompályák négy elektronja a kötés pi1 és pi2 Mo-jába kerül. Mivel a pi1 konstruktív kölcsönhatást tartalmaz a C2 és a C3 között, az 1,3-butadién molekulában van egy olyan pi-kötési kölcsönhatás e két karbon között, amely rövidebb hosszúságát és a forgás akadályát jelenti. Az 1,3-butadién valenciakötvény-képe azt mutatja, hogy a két pi kötés egymástól elszigetelt, mindegyik pi elektron pár “beragadt” a saját pi-kötésében. A molekuláris orbitális elmélet azonban (Pontosan) azt jósolja, hogy a négy pi elektron bizonyos mértékig delokalizálódik vagy “szétterül” az egész pi rendszeren.

1,3-butadién a konjugált pi kötések rendszerének legegyszerűbb példája. Ahhoz, hogy konjugáltnak lehessen tekinteni, két vagy több pi kötést csak egyetlen kötéssel kell elválasztani – más szóval, nem lehet beavatkozó sp3-hibridizált szén, mert ez lebontaná a párhuzamos p pályák átfedő rendszerét. Az alábbi vegyületben például a C1-C2 és C3-C4 kettős kötések konjugálódnak, míg a C6-C7 kettős kötést a másik két pi kötésből SP3-hibridizált C5 izolálja.

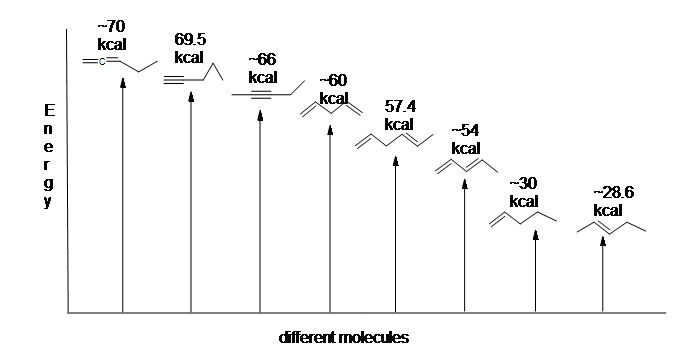
egy nagyon fontos koncepció, amelyet szem előtt kell tartani, az, hogy van egy inherens termodinamikai stabilitás a konjugációval kapcsolatban. Ez a stabilitás kísérletileg mérhető két különböző dién hidrogénezésének hőjével összehasonlítva. (A hidrogénezés egy olyan reakciótípus,amelyről sokkal többet fogunk megtudni a 15. fejezetben: lényegében egy hidrogénmolekula – két proton és két elektron – hozzáadásának folyamata egy P kötéshez). Amikor az 1,3-pentadién két konjugált kettős kötése “hidrogénezett” pentán előállítására, körülbelül 225 kJ szabadul fel egy mól pentán képződik. Hasonlítsa össze ezt a körülbelül 250 kJ/mol felszabadulással, amikor az 1,4-pentadién két izolált kettős kötése hidrogénezett, szintén pentánt képezve.
a diénekből, például 1,3-butadiénből és izoprénből származó szintetikus polimerek képződését a 18.5 pont tárgyalja. A szintetikus polimerek nagy molekulák, amelyek kisebb ismétlődő egységekből állnak. Ön valószínűleg kissé ismeri számos ilyen polimerek; például, polietilén, polipropilén, polisztirol, poli (vinil-klorid).

13.6.ábra: 1,3-butadién hidrogénezésére szolgáló energiagráf (nem skálázható).
a hidrogénezés 1,3-butadién-kibocsátás kevesebb, mint a becsült energia mennyisége, az energia-tartalma 1,3-butadién lehet alacsonyabb, mint vártunk. Más szóval, az 1,3-butadién stabilabb, mint a képlete.
a konjugált dién energiája alacsonyabb: más szóval stabilabb. Általában a konjugált pi kötések stabilabbak, mint az izolált pi kötések.
ez Itt egy energia ábra összehasonlítja a különböző típusú kötvények a felmelegíti a hidrogénezés (egy tégla) megmutatni viszonylagos stabilitás minden molekula (1 kcal = 4.18 kJ). (Minél alacsonyabb a hidrogénezés hője (pi kötésenként), annál stabilabb a szerkezet.)
a diének konjugációval történő stabilizálása kevésbé drámai, mint a benzol aromás stabilizálása. Ennek ellenére a konjugáció hasonló rezonancia és molekuláris orbitális leírása írható.
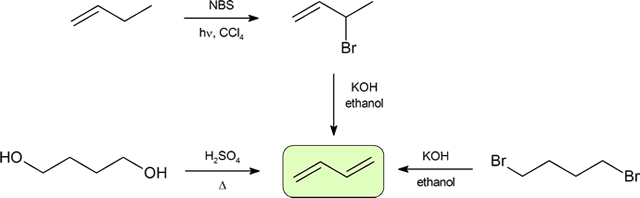
diének szintézise
a konjugált diének szintézisének két leggyakoribb módja az alkoholok dehidrogénezése és az organohalidok dehidrohalogénezése, amelyeket alkének előállítása során vezettek be (9.9 pont). A következő séma szemlélteti a konjugált dién előkészítésének néhány módját.
konjugált pi rendszerek tartalmazhatnak oxigén-és nitrogénatomokat, valamint szenet. A zsírmolekulák metabolizmusában a legfontosabb reakciók közé tartoznak a karbonilcsoportokhoz konjugált alkének.

A Mo elmélet nagyon hasznos annak magyarázatában, hogy a konjugált pi kötések kiterjesztett rendszereit tartalmazó szerves molekulák gyakran megkülönböztető színekkel rendelkeznek. a béta-karotin, a sárgarépa narancssárga színéért felelős vegyület, kiterjesztett rendszere 11 konjugált pi kötés.

gyakorlatok
2.9 gyakorlat: Azonosítsa az összes konjugált és izolált kettős kötést az alábbi struktúrákban. Minden konjugált pi-rendszerhez adja meg az átfedő p-pályák számát, valamint azt, hogy hány pi elektron oszlik meg közöttük.

2.10. gyakorlat: azonosítsa az összes izolált és konjugált pi kötést likopinban, a vörös színű vegyületet paradicsomban. Hány pi elektron található a konjugált pi rendszerben?
Leave a Reply