사이의 차이 하나의 더블 트리플 채권
주요한 차이가–단 하나 대중 vs 트리플 채권
화학 채권 보유 원자 분자에 의해 함께 설치 사이의 힘은 전자 및 핵의 두 개의 원자를 함유하고 있습니다. 화학 반응은 화학 결합을 확립하거나 끊음으로써 규율됩니다. 공유 결합,이온,반 데르 왈 등과 같은 다양한 유형의 결합이 있습니다. 의 속성이 채권에 따라 다양한 측면에 등 자연의 분자,고체형(결정 또는 비정질)등입니다. 공유 결합은 두 개 이상의 전자를 공유함으로써 형성된다. 의 수를 공유하는 전자 사이에 원자 수를 결정의 채권 여부,그것은 단일,이중 또는 삼중. 따라서 단일,이중 및 삼중 결합은 공유 결합입니다. 단일 이중 결합과 삼중 결합의 주요 차이점은 공유 전자의 수입니다. 는 경우 공유된 수은 한 쌍의 전자가 채권 될 것입니다 단일 결합하면 두 원자가 결합에 의해 두 쌍(네 개의 전자),그것을 형성할 것입니다중 결합. 삼중 결합은 전자의 3 쌍(6 개의 원자)을 공유함으로써 형성된다. 이러한 공유 전자는 일반적으로 원자가 전자로 알려져 있습니다. 이 기사에서는
1 을 살펴볼 것입니다. 단일 채권이란 무엇입니까?
-정의,속성,예
2. 이중 결합이란 무엇입니까?
-정의,속성,예
3. 삼중 결합이란 무엇입니까?
-정의,속성,예
4. 단일 이중 결합과 삼중 결합의 차이점은 무엇입니까?
무엇을 하나의 채권
단일 결합에 의해 형성되는 공유의 한 쌍의 원자의 전자 사이에 인접한 두 개의 원자를 함유하고 있습니다. 단일 결합은 각 원자가 하나의 원자가 전자를 제공하는 공유 결합의 가장 간단한 형태입니다. 이 원자가 전자는 원자의 가장 바깥 쪽 껍질에 위치하고 있습니다. 여기서,음전하를 띤 공유 전자는 원자의 양전하를 띤 핵에 의해 끌어 당겨지고 있습니다. 이 당기는 힘은 원자를 함께 잡습니다. 이 배열은 단일 결합으로 알려져 있습니다. 단일 결합을 갖는 분자는 다중 결합을 갖는 분자와 달리 반응성이 적다. 또한,그들은 보다 약한 여러 유대와 높은 유대 길이 때문에 당기는 힘을 최소화하 여 적은 힘으로 간에 원자에 비교하면 여러 개 있습니다. 단일 결합으로 표시는 단 하나의 대;ex:C C. 의 경우 같은 메탄,에탄,프로판에는 몇 가지 예는 화합물에 대한 단일 수 있습니다.
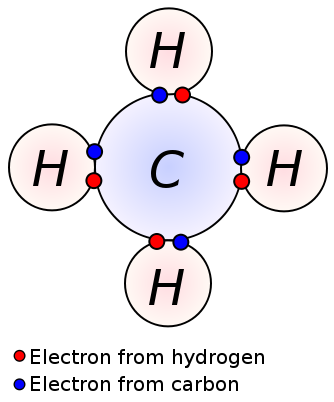
메탄
What is a Double Bond
이중 결합에 의해 형성된 공유 두 쌍의 원자의 전자에 위치한 궤도 가장 바깥쪽의 원자를 함유하고 있습니다. 이중 결합을 갖는 화합물은 단일 결합 된 화합물보다 반응성이 높지만 삼중 결합을 갖는 화합물보다 반응성이 적다. 이중 결합은 두 개의 평행 한 대시로 표시됩니다. 몇 가지 예는 화합물의 이중 결합을 포함 된 외과 같은 에틸렌,프로필렌,카르보닐 화합물(C=O),azo 화합물(N=N),imines(C=N)및 sulfoxides(S=O).
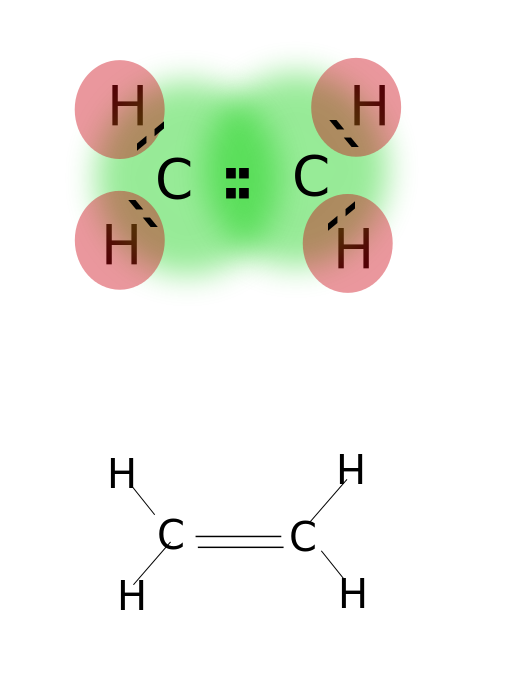
에틸렌
무엇이 트리플 채권
경우 두 원자가 공유하는 세 쌍의 원자의 전자(여섯 원자의 전자),설립된 채권이라고 트리플 채권. 삼중 결합은 가장 강하고 반응성이 강한 공유 결합입니다. 과 비교했을 때 단일 및 이중 채권,트리플 채권 가장 낮은 채권 길이로 인해 더 높은 힘을 당 사이에 두 개의 원자를 함유하고 있습니다. 트리플 본드로 표시되어 있는 세 개의 병렬시 사이에 두 개의 원자;ex:C≡C. 의 몇 가지 예는 화합물과 트리플 채권을 포함하는 질소 가스(N≡N),시안화물이온(C≡N),아세틸렌(CH≡CH)그리고 일산화탄소(C≡O).
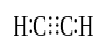
아세틸렌
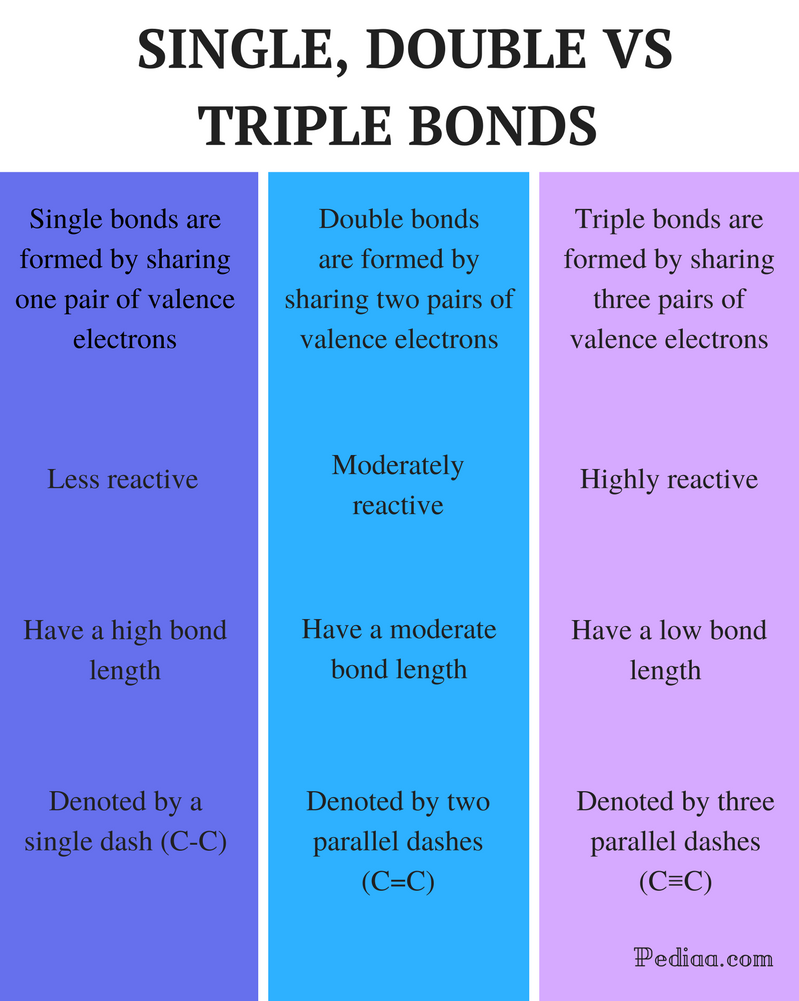
사이의 차이 하나의 더블 트리플 채권
정의:
단일 결합: 하나의 결합은 한 쌍의 원자가 전자를 공유함으로써 형성된다.
이중 결합:이중 결합은 두 쌍의 원자가 전자를 공유함으로써 형성된다.
삼중 결합:삼중 결합은 3 쌍의 원자가 전자를 공유함으로써 형성된다.
반응성:
단일 결합:단일 결합은 반응성이 적습니다.
이중 결합:이중 결합은 적당히 반응성이 있습니다.
삼중 결합:삼중 결합은 반응성이 높습니다.
결합 길이:
단일 결합:단일 결합은 높은 결합 길이를 갖는다.
이중 결합:이중 결합은 적당한 결합 길이를 갖는다.
트리플 본드: 삼중 결합은 낮은 결합 강도를 갖는다.
로 표시:
단일 결합:단일 결합은 단일 대시(C-C)로 표시됩니다.
이중 결합:이중 결합은 두 개의 평행 대시(C=C)로 표시됩니다.
삼중 결합:삼중 결합은 3 개의 평행 대시(C≡C)로 표시됩니다.
예:
단일 결합:예의 경우 같은 메탄,에탄,프로판,부탄 etc.
이중 결합:예로는 에틸렌,프로펜,카르보닐 화합물(C=O),아조 화합물(N=N),이민(C=N),및 설폭사이드(S=O)가 있다.
트리플 본드: 예로는 질소 가스(N≡N),시안화물 이온(C≡N),아세틸렌(CH≡CH)및 일산화탄소(C≡O)가 있습니다.
![]()
Leave a Reply