Nieuws-congenitale leukemie na zwaar gebruik van permethrinspray tijdens de zwangerschap

casus REPORT
congenitale leukemie na zwaar gebruik van permethrinspray tijdens de zwangerschap
A Borkhardt, M Wilda, u Fuchs, L Gortner en I Reiss
Children ‘ s University Hospital Giessen, Feulgenstr 12, 35392 Giessen, Duitsland
correspondentie met: Dr.Borkhardt, pediatrische hematologie en oncologie, Feulgenstr 12, 35392 Giessen, Duitsland; Arndt.borkhardt{at}paediat.med.uni-giessen.de
aanvaard 6 oktober 2002
ABSTRACT
Een enkel geval wordt beschreven van congenitale leukemie met 11q23 / ml herschikking bij een te vroeg geboren vrouwelijke pasgeborene. Vanwege arachnofobie had de moeder permethrin, een veel gebruikt insecticide voor huishoudelijk gebruik, zwaar misbruikt. Permethrin wordt beschouwd als relatief veilig, maar, gezien de geschiedenis van de moeder, werd zijn potentieel getest om splitsing van het MLL-gen in celcultuur te veroorzaken. Incubatie van de bv173-cellijn met 50 µM permethrin veroorzaakte gemakkelijk MLL-splitsing.
trefwoorden: congenitale leukemie; leukemie; permethrin; insecticide; 11q23/MLL
congenitale leukemie is een zeldzame ziekte die ongeveer één op de 200 000-250 000 levendgeborenen per jaar treft. Ondanks zijn zeldzaamheid, heeft aangeboren leukemie veel interesse gestimuleerd vanwege de mogelijkheid om meer te leren over de onderliggende oorzaken van in utero leukemogenese. Er zijn vele risicofactoren die de kans op vroege inductie van een leukemisch fenotype kunnen verhogen—bijvoorbeeld, ouderlijke blootstelling aan beroepsmatige en milieu toxines, gebruik van tabak, marihuana, alcohol, en andere toxines.1 congenitale leukemie en kinderleukemie worden vaak geassocieerd met herschikkingen van het MLL-gen bij chromosoom 11q23.2 verschillende stoffen zijn onderzocht op hun potentieel om de placentabarrière te passeren en een dergelijke chromosomale breuk bij 11q23/MLL te induceren.3,4
hier wordt de lijst uitgebreid van geneesmiddelen die het MLL-gen kunnen splitsen, tenminste wanneer cellen in cultuur worden blootgesteld. Samen met een nogal ongewone case geschiedenis, onze experimentele gegevens werpen enig licht op de generatie van aangeboren leukemie en kunnen helpen om een aantal van de fatale gevallen van deze ziekte te voorkomen. een 27-jarige gezonde vrouw werd toegelaten tot de afdeling gynaecologie vanwege vroegtijdige bevalling. Ze was in de 35e week van haar eerste zwangerschap. Prenatale controles waren normaal. Aangezien het cardiotocogram geen foetaal hartritme liet zien, werd een keizersnede in noodgevallen gepland. Zes minuten later beviel de vrouw echter spontaan van een prematuur kind met een gewicht van 2300 g en geen vitale functies, maar een opvallende heldere huidskleur. Primaire cardiopulmonale reanimatie werd onmiddellijk gestart met endotracheale intubatie, borstcompressie en herhaalde toediening van adrenaline. De Apgar-score bleef echter 0 na vijf en tien minuten. Het pediatrische noodteam arriveerde 10 minuten later en bleef cardiopulmonale reanimatie uitvoeren. Een centrale lijn werd bereikt door katheterisatie van de navelader. 25 minuten na de partum werd een stabiele bloedsomloop vastgesteld, met een hartslag van 140 slagen / min. Een lichamelijk onderzoek toonde hepatomegalie van 5 cm onder de kustrand en nodulaire livid infiltraties van de huid (fig 1A hieronder).
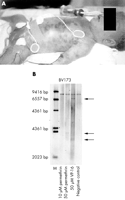
| figuur 1 (A) de patiënt op de leeftijd van 2 uur. Let op de leukemische huidinfiltratie (“bosbessenvlekken”). B) Zuidelijke vlek met een MLL-herschikking in de bv173-cellijn geïncubeerd met 50 µM permethrin gedurende zes uur. VP16 geïnduceerde MLL splitsing werd gebruikt als een controle. |
afgezien van de normale anatomie van het hart, vertoonde de echografie aanzienlijke pulmonale hypertensie in combinatie met tweede tot derde graad insufficiëntie van de tricuspidalisklep. Naast hepatomegalie werd een bilaterale intracraniale bloeding gevonden. Voor voldoende oxygenatie en verwijdering van koolstofdioxide was hoogfrequente ventilatie nodig met 10 Hz, FIO2 = 1, en een gemiddelde luchtwegdruk van 13 cm H2O. het eerste aantal witte bloedcellen was 400 000 / µl met een overmaat aan myeloïde blastcellen. Het onderzoek van het beendermerg bevestigde de diagnose van een aangeboren scherpe myeloid leukemie, met 95% blast cellen van myelomonocytic morfologie (FAB-M5). Een volledige bloeduitwisseling werd uitgevoerd, die het aantal witte bloedcellen verminderde tot 56 000 / µl en resulteerde in een verbetering van de oxygenatie en ventilatie. Twaalf uur later was het aantal witte bloedcellen weer gestegen tot 125 000/µl. Extracorporale membraanoxygenatie werd overwogen, maar werd uiteindelijk afgewezen vanwege de progressieve intracraniale bloeding waarbij een groot gebied van het parenchym betrokken was. Het kind stierf 48 uur na de geboorte aan multi-orgaanfalen. Afgezien van de ernstige hersenbeschadiging al gediagnosticeerd door echografie, de autopsie toonde diffuse infiltratie van longen, lever, milt, en cutis.
CELCULTUUREXPERIMENTEN: inductie van MLL-herschikkingen door PERMETHRIN
De experimentele test werd precies uitgevoerd zoals beschreven door Strick et al.3 die een breed scala van natuurlijke stoffen in voedsel en voedingssupplementen analyseerden op hun vermogen om plaatsspecifieke splitsing binnen het MLL-gen te induceren.
resultaten en discussie
cytogenetische analyse van het beenmergaspiraat toonde de aanwezigheid van een translocatie t(11;19)(q23;p13) in alle geanalyseerde metafasen. Verder toonden we een herschikking van het MLL oncogeen op chromosoom 11q23 door Zuidelijke bevleking. Routine immunophenotyping toonde expressie van CD15, CD33, CD 65s, en MPO (gegevens niet getoond). In eerdere studies kwam het monoklonale antilichaam 7.1 naar voren als een waardevol immunofenotypisch hulpmiddel voor de detectie van leukemische cellen, met NG2-antigeenexpressie die sterk correleert met MLL-herschikkingen bij zuigelingen.5,6 in ons geval, echter, bleef het bevlekken met dit monoclonal antilichaam negatief, wat ons verhinderde verdere experimenten van het sorteren van cellen uit te voeren.
de moeder had blijkbaar al sinds de vroege kindertijd last van arachnofobie. Twee jaar voor haar zwangerschap begon ze overmatig permethrin te gebruiken. Sindsdien woonde ze alleen. Mensen vermeden haar te bezoeken vanwege de penetrerende geur in haar huis. Permethrin is een veel gebruikt insecticide dat bescherming biedt tegen de malariavectoranofeles.7,8 het is ook bekend als een effectief medicijn tegen schurft en de hoofdluis Pediculosis capitis.9,10 vergeleken met andere geneesmiddelen, wordt het als veilig beschouwd en het actuele gebruik ervan wordt zelfs aanbevolen voor pasgeborenen met schurft.Het is echter in verband gebracht met het ontstaan van zowel chromosomale afwijkingen in beenmergcellen van muizen als DNA-laesies in menselijke lymfocyten.12-14 we veronderstelden daarom dat permethrin de placenta van de zwangere vrouw passeerde en de hematopoëtische precursorcellen in de zich ontwikkelende foetus beïnvloedde, resulterend in leukemogenese. We hebben daarom geprobeerd om de herschikkingen binnen het MLL oncogeen in vitro te genereren door bv173 cellen bloot te stellen aan 50 µM permethrin. Na 24 uur blootstelling vertoonden de met permethrin behandelde bv173-cellen een duidelijke MLL-herschikking, terwijl de onbehandelde cellen alleen het wild type MLL-gen vertoonden (fig.1B hierboven). Daarom raden we grote voorzichtigheid aan bij het gebruik van permethrin tijdens de zwangerschap. Zelfs als definitieve conclusies niet kunnen worden getrokken uit een enkel geïsoleerd geval, onze gegevens suggereren sterk dat permethrin ernstige bijwerkingen kan hebben wanneer foetale hematopoëtische precursor cellen worden blootgesteld in utero. In dezelfde geest blijkt uit een recent rapport van een multinationale samenwerking dat het gebruik van muggenbestrijdende geneesmiddelen tijdens de zwangerschap in belangrijke mate geassocieerd is met leukemie bij zuigelingen.4 Het is bijzonder opmerkelijk dat de auteurs vonden deze vereniging alleen voor de MLL herschikte gevallen en niet voor MLL germline gevallen. Dit pleit sterk tegen selectie bias in hun case-control studie en ondersteunt de hypothese dat in utero blootstelling de MLL herschikkingen veroorzaakt.
ten slotte werd de moeder in ons geval met succes behandeld voor arachnofobie door middel van psychotherapie. Twee jaar later beviel ze van een gezonde term jongen die geen klinische tekenen van leukemie had en die nog steeds gezond is op de leeftijd van 13 maanden.dankbetuigingen deskundige technische bijstand van Claudia Keller en Stefanie Garkisch wordt dankbaar erkend. Wij danken Jochen Harbott, Giessen, Duitsland voor het verstrekken van de cytogenetische gegevens. Immunofenotypische gegevens werden verstrekt door W-D Ludwig, Robert Rössle Cancer Centre, Humboldt University, Berlijn, Duitsland. De moleculaire studies werden ondersteund door de Duitse Kankerstichting (subsidie 10-1658-Bo2).
- Sande JE, Arceci RJ, Lampkin BC. Aangeboren en neonatale leukemie. Semin Perinatol 1999; 23: 274-85. Ford AM, Ridge SA, Cabrera me, et al. In utero herschikkingen in het trithorax-gerelateerde oncogeen bij kinderleukemieën. Natuur 1993; 363:358–60.
- Strick R, Strissel PL, Borgers S, et al. Bioflavonoïden uit de voeding induceren een splitsing in het MLL-gen en kunnen bijdragen aan leukemie bij zuigelingen. Proc Natl Acad Sci USA 2000; 97: 4790-5. Alexander FE, Patheal SL, Biondi A, et al. Transplacental chemische blootstelling en risico van kinderleukemie met MLL genfusie. Cancer Res 2001; 61: 2542-6. Smith FO, Rauch C, Williams De, et al. De humane homoloog van rat NG2, een chondroïtinesulfaat proteoglycaan, wordt niet uitgedrukt op het celoppervlak van normale hematopoëtische cellen, maar wordt uitgedrukt door acute myeloïde leukemie blasten van slechte prognose patiënten met afwijkingen van chromosoom band 11q23. Blood 1996; 87: 1123-33.
- Behm FG, Smith FO, Raimondi SC, et al. Humane homoloog van het ratchondroïtinesulfaat proteoglycan, NG2, gedetecteerd door monoklonaal antilichaam 7.1, identificeert acute lymfatische leukemieën uit de kindertijd met T(4;11)(q21;q23) of t(11;19)(q23;p13) en MLL gen herschikkingen. Blood 1996; 87: 1134-9.
- Rowland M, Durrani N, Hewitt S, et al. Permethrin-behandelde chaddars en top-sheets: geschikte technologie voor bescherming tegen malaria in Afghanistan en andere complexe noodsituaties. Trans R Soc Trop Med Hyg 1999; 93: 465-72.
- Binka FN, Mensah OA, Mills A. the cost-effectiveness of permethrin impregned bednets in preventing child mortality in Kassena-Nankana district of Northern Ghana. Gezondheidsbeleid 1997; 41: 229-39. Blanshard ME, Schofield J. Scabies: a practical approach. Prof Zorg Moeder Kind 1999; 9: 15-16.
- Dodd CS. Ingrepen voor de behandeling van Hals. Cochrane Database Syst Rev 2000; CD001165. Quarterman MJ, Lesher JL, Jr. neonatale schurft behandeld met permethrin 5% crème. Pediatr Dermatol 1994; 11: 264-6.
- Cantalamessa F. Acute toxiciteit van twee pyrethroïden, permethrin en cypermethrin bij neonatale en volwassen ratten. Arch Toxicol 1993; 67: 510-13.
- Barrueco C, Herrera A, Caballo C, et al. Inductie van structurele chromosoomafwijkingen in humane lymfocytenculturen en CHO-cellen door permethrin. Teratog Carcinog Mutagen 1994; 14: 31-8.
- Santoni G, Cantalamessa F, Spreghini E, et al. Veranderingen in de distributie en functies van T-cellen bij prenataal aan cypermethrin blootgestelde ratten: mogelijke betrokkenheid van catecholamines. Toxicology 1999; 138: 175-87.
Leave a Reply