Health Knowledge
MERK:
Vi er for tiden i ferd med å oppdatere dette kapittelet, og vi setter pris på tålmodigheten din mens dette blir fullført.
Bias i Epidemiologiske Studier
Selv om resultatene fra en epidemiologisk studie kan gjenspeile den virkelige effekten av eksponering (er) på utviklingen av utfallet som undersøkes, bør det alltid vurderes at funnene faktisk kan skyldes en alternativ forklaring1.slike alternative forklaringer kan skyldes effektene av tilfeldighet( tilfeldig feil), skjevhet eller forvirring som kan gi falske resultater, noe som fører oss til å konkludere eksistensen av en gyldig statistisk forening når man ikke eksisterer eller alternativt fraværet av en forening når man virkelig er til stede1.
Observasjonsstudier er spesielt utsatt for effektene av tilfeldighet, skjevhet og forvirring, og disse faktorene må vurderes både i design-og analysefasen av en epidemiologisk studie slik at deres effekter kan minimeres.Bias kan defineres som enhver systematisk feil i en epidemiologisk studie som resulterer i et feilaktig estimat av den sanne effekten av en eksponering på utfallet av interesse.1
- Bias skyldes systematiske feil i forskningsmetodikken.
- effekten av bias vil være et estimat enten over eller under den sanne verdien, avhengig av retningen til den systematiske feilen.
- størrelsen på bias er generelt vanskelig å kvantifisere, og det er begrenset omfang for justering av de fleste former for bias på analysetrinnet. Som et resultat er nøye vurdering og kontroll av måtene som bias kan innføres under utformingen og gjennomføringen av studien, avgjørende for å begrense effektene på studieresultatets gyldighet.Vanlige typer bias i epidemiologiske studier
Mer enn 50 typer bias har blitt identifisert i epidemiologiske studier, men for enkelhets skyld kan de grovt grupperes i to kategorier: informasjonsbias og seleksjonsbias.
1. Informasjonsbias
informasjonsbias er resultat av systematiske forskjeller i måten data om eksponering eller utfall er hentet fra de ulike studiegruppene.1 dette kan bety at enkeltpersoner blir tildelt feil utfallskategori, noe som fører til et feil estimat av sammenhengen mellom eksponering og utfall.
Feil i målingen er også kjent som feilklassifikasjoner, og størrelsen på effekten av bias avhenger av typen feilklassifisering som har oppstått. Det finnes to typer feilklassifisering – differensial og ikke-differensial-og disse behandles andre steder (se «Variasjonskilder, måling og kontroll»).
Observatørskjevhet kan være et resultat av utprøverens forkunnskaper om hypotesen som undersøkes, eller kunnskap om individets eksponering eller sykdomsstatus. Slik informasjon kan påvirke måten informasjon samles inn, måles eller tolkes av utprøveren for hver av studiegruppene.for eksempel, i en studie av en ny medisin for å behandle hypertensjon, hvis utprøveren er klar over hvilken behandlingsarm deltakere ble allokert til, kan dette påvirke deres lesing av blodtrykksmålinger. Observatører kan undervurdere blodtrykket hos de som har blitt behandlet, og overvurdere det hos de i kontrollgruppen.
intervjuerens bias oppstår når en intervjuer stiller ledende spørsmål som systematisk kan påvirke svarene gitt av intervjuobjektene.
Minimerer bias mellom observatører og intervjuere:
- der det er mulig, bør observatører være blindet for eksponering og sykdomsstatus hos den enkelte
- Blinde observatører til hypotesen som undersøkes.
- I en randomisert kontrollert studie blinde etterforskere og deltakere til behandling og kontrollgruppe (dobbeltblindende).
- Utvikling av en protokoll for innsamling, måling og tolkning av informasjon.
- Bruk av standardiserte spørreskjemaer eller kalibrerte instrumenter, for eksempel blodtrykksmålere.
- Opplæring av intervjuere.
Tilbakekalling (eller respons) bias-i en case-control studie data om eksponering er samlet i ettertid. Kvaliteten på dataene bestemmes derfor i stor grad av pasientens evne til nøyaktig å huske tidligere eksponeringer. Tilbakekallingsskjevhet kan oppstå når informasjonen om eksponering varierer mellom tilfellene og kontrollene. For eksempel kan en person med utfallet under undersøkelse (sak) rapportere sin eksponeringserfaring annerledes enn en person uten utfallet (kontroll) under undersøkelse.
Tilbakekallingsskjevhet kan føre til enten undervurdering eller overvurdering av sammenhengen mellom eksponering og utfall.
Metoder for å minimere tilbakekallingsskjevhet inkluderer:
- Innsamling av eksponeringsdata fra arbeid eller medisinske journaler.
- Blindende deltakere til studiehypotesen.Sosial ønskelighet skjevhet oppstår der respondentene til undersøkelser har en tendens til å svare på en måte de føler vil bli sett på som gunstig av andre, for eksempel ved over-rapportering positiv atferd eller under-rapportering uønskede seg. I rapportering skjevhet, enkeltpersoner kan selektivt undertrykke eller avsløre informasjon, av lignende grunner (for eksempel rundt røyking historie). Rapporteringsskjevhet kan også referere til selektiv utfallsrapportering av studieforfattere.
Performance bias refererer til når studiepersonell eller deltakere endrer atferd / svar der de er klar over gruppetildelinger.
Detection bias oppstår der måten utfallsinformasjon samles inn på, varierer mellom grupper. Instrument bias refererer til hvor et utilstrekkelig kalibrert måleinstrument systematisk over / undervurderer måling. Blinding av utfallsvurderere og bruk av standardiserte, kalibrerte instrumenter kan redusere risikoen for dette.
2. Seleksjonsbias
seleksjonsbias oppstår når det er en systematisk forskjell mellom Enten:
- De Som deltar i studien og de som ikke gjør det (påvirker generaliserbarhet) eller
- De i behandlingsarmen i en studie og de i kontrollgruppen (påvirker sammenlignbarhet mellom gruppene).
Det vil si at det er forskjeller i egenskapene mellom studiegrupper, og disse egenskapene er relatert til enten eksponering eller utfall under undersøkelse. Utvalg bias kan oppstå for en rekke årsaker.
Sampling bias beskriver scenariet der noen individer i en målgruppe er mer sannsynlig å bli valgt for inkludering enn andre. For eksempel, hvis deltakerne blir bedt om å frivillig for en studie, er det sannsynlig at de som frivillig ikke vil være representative for den generelle befolkningen, og truer generaliserbarheten av studieresultatene. Frivillige har en tendens til å være mer helsebevisste enn den generelle befolkningen.
Allokeringsskjevhet oppstår i kontrollerte studier når det er en systematisk forskjell mellom deltakerne i studiegruppene (annet enn intervensjonen som studeres). Dette kan unngås ved randomisering.
Tap av oppfølging er et spesielt problem knyttet til kohortstudier. Bias kan innføres dersom personene som er tapt for oppfølging, avviker med hensyn til eksponering og utfall fra de personene som forblir i studien. Det differensielle tapet av deltakere fra grupper i en randomisert kontrollstudie er kjent som utmattelsesbias.
• Seleksjonsbias i case-control studier
Seleksjonsbias er et spesielt problem som ligger i case-control studier, hvor Det gir opphav til ikke-sammenlignbarhet mellom saker og kontroller. I case-control-studier bør kontroller trekkes fra samme populasjon som tilfellene, slik at de er representative for befolkningen som produserte tilfellene. Kontroller brukes til å gi et estimat av eksponeringsgraden i befolkningen. Seleksjonsskjevhet kan derfor oppstå når de individer som er valgt som kontroller, ikke er representative for populasjonen som produserte tilfellene.
potensialet for seleksjonsskjevhet i case-control studier er et spesielt problem når saker og kontroller rekrutteres utelukkende fra sykehus eller klinikker. Slike kontroller kan være å foretrekke av logistiske årsaker. Imidlertid har sykehuspasienter en tendens til å ha forskjellige egenskaper til den bredere befolkningen, for eksempel kan de ha høyere nivåer av alkoholforbruk eller sigarettrøyking. Deres opptak til sykehus kan til og med være relatert til eksponeringsstatus, så målinger av eksponering blant kontroller kan være forskjellig fra referansepopulasjonen. Dette kan resultere i et partisk estimat av sammenhengen mellom eksponering og sykdom.for eksempel, i en case-control studie som undersøker effekten av røyking på lungekreft, ville styrken av foreningen bli undervurdert dersom kontrollene var pasienter med andre forhold på luftveiene, fordi opptak til sykehus for andre lungesykdommer også kan være relatert til røykestatus. Mer subtilt kan effekten av alkohol på leversykdom potensielt undervurderes dersom kontroller tas fra andre avdelinger: høyere enn gjennomsnittlig alkoholforbruk kan føre til opptak for en rekke andre forhold, for eksempel traumer.da potensialet for seleksjonsskjevhet sannsynligvis vil være mindre av et problem i populasjonsbaserte case-control-studier, kan nabolagskontroller være et foretrukket valg når man bruker tilfeller fra sykehus eller klinikk. Alternativt kan potensialet for utvalgsskjevhet minimeres ved å velge kontroller fra mer enn en kilde. For eksempel, bruk av både sykehus og nabolag kontroller.
• Seleksjonsbias i kohortstudier
seleksjonsbias kan være mindre problem i kohortstudier sammenlignet med case-control-studier, fordi eksponerte og ueksponerte individer er inkludert før de utvikler utfallet av interesse.
seleksjonsskjevhet kan imidlertid innføres når fullstendigheten av oppfølging eller case-konstatering varierer mellom eksponeringskategorier. Det kan for eksempel være lettere å følge opp eksponerte personer som alle jobber i samme fabrikk, enn ueksponerte kontroller valgt fra fellesskapet (tap til oppfølgingsskjevhet). Dette kan minimeres ved å sikre at det opprettholdes et høyt oppfølgingsnivå blant alle studiegrupper.
healthy worker-effekten er en potensiell form for seleksjonsskjevhet som er spesifikk for yrkeskohortstudier. For eksempel kan en yrkeskohortstudie søke å sammenligne sykdomsrater blant individer fra en bestemt yrkesgruppe med individer i en ekstern standardpopulasjon. Det er en risiko for skjevhet her fordi personer som er ansatt generelt må være sunn for å arbeide. I motsetning vil den generelle befolkningen også inkludere de som er uegnet til å jobbe. Derfor kan dødelighet eller sykelighet i yrkesgruppekohorten være lavere enn i befolkningen som helhet.
for å minimere potensialet for denne formen for skjevhet, bør en sammenligningsgruppe velges fra en gruppe arbeidstakere med forskjellige jobber utført på forskjellige steder i en enkelt fasilitet1; for eksempel en gruppe ikke-eksponerte kontorarbeidere. Alternativt kan sammenligningsgruppen velges fra en ekstern populasjon av sysselsatte personer.
• Seleksjonsskjevhet i randomiserte studier
Randomiserte studier er teoretisk mindre sannsynlig å bli påvirket av seleksjonsskjevhet, fordi individer er tilfeldig allokert til gruppene som sammenlignes, og det bør iverksettes tiltak for å minimere muligheten for etterforskere eller deltakere til å påvirke denne tildelingsprosessen. Avslag på å delta i en studie, eller påfølgende uttak, kan imidlertid påvirke resultatene dersom årsakene er relatert til både eksponering og utfall.
Confounding
Confounding, interaksjon og effekt modifikasjon
Confounding gir en alternativ forklaring på en sammenheng Mellom en eksponering (X) og et utfall. Det oppstår når en observert forening faktisk er forvrengt fordi eksponeringen også er korrelert med en annen risikofaktor (Y). Denne risikofaktoren Y er også forbundet Med utfallet, men uavhengig Av eksponeringen som undersøkes, X. som en konsekvens er den estimerte assosiasjonen ikke den samme som den sanne effekten av eksponering X på utfallet.
en ulik fordeling Av den ekstra risikofaktoren, Y, mellom studiegruppene vil resultere i forvirrende. Den observerte sammenhengen kan helt eller delvis skyldes effekten av forskjeller mellom studiegruppene i stedet for eksponeringen som undersøkes.1
en potensiell confounder er en faktor som kan ha en effekt på risikoen for sykdom under studien. Dette kan omfatte faktorer med direkte årsakssammenheng til sykdommen, samt faktorer som er proxytiltak for andre ukjente årsaker, som alder og sosioøkonomisk status.2
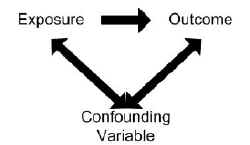
for at en variabel skal betraktes som en confounder:
- variabelen må være uavhengig forbundet med utfallet (dvs.være en risikofaktor).
- variabelen må også knyttes til eksponeringen i kildepopulasjonen under studien.
- variabelen skal ikke ligge på årsakssammenheng mellom eksponering og sykdom.
Eksempler på confounding
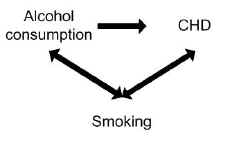
en studie fant at alkoholforbruk var forbundet med risikoen for koronar hjertesykdom (CHD). Røyking kan imidlertid ha forvirret sammenhengen mellom alkohol og CHD.Røyking er en risikofaktor i seg selv for CHD, så er uavhengig forbundet med utfallet, og røyking er også forbundet med alkoholforbruk fordi røykere har en tendens til å drikke mer enn ikke-røykere.Å Kontrollere for den potensielle forvirrende effekten av røyking kan faktisk ikke vise noen sammenheng mellom alkoholforbruk og CHD.
Effekter av konfunderende
Konfunderende faktorer, hvis de ikke er kontrollert for, forårsaker skjevhet i estimatet av virkningen av eksponeringen som studeres. Effektene av confounding kan resultere i:
- en observert forening når ingen reell forening eksisterer.
- Ingen observert forening når en sann forening eksisterer.
- en undervurdering av foreningen (negativ confounding).
- en overvurdering av foreningen (positiv confounding).
Controlling for confounding
Confounding kan tas opp enten på studiedesign scenen, eller justert for på analysestadiet å gi tilstrekkelig relevante data er samlet inn. En rekke metoder kan brukes til å kontrollere for potensielle confounding faktorer og målet med dem alle er å gjøre gruppene så like som mulig med hensyn til confounder (s).
Kontrollere for confounding på designstadiet
Potensielle confounding faktorer kan identifiseres på designstadiet basert på tidligere studier eller fordi en kobling mellom faktor og utfall kan betraktes som biologisk plausibelt. Metoder for å begrense confounding på designstadiet inkluderer randomisering, begrensning og matching.
• Randomisering
Dette er den ideelle metoden for å kontrollere for confounding fordi alle potensielle confounding variabler, både kjente og ukjente, skal fordeles likt mellom studiegruppene. Det innebærer tilfeldig tildeling (f.eks. ved hjelp av en tabell med tilfeldige tall) av individer for å studere grupper. Denne metoden kan imidlertid kun brukes i eksperimentelle kliniske studier.
• Begrensning
Begrensning begrenser deltakelse i studien til personer som er like i forhold til confounder. For eksempel, hvis deltakelse i en studie er begrenset til ikke-røykere, vil enhver potensiell forstyrrende effekt av røyking bli eliminert. En ulempe med begrensning er imidlertid at det kan være vanskelig å generalisere resultatene av studien til den bredere befolkningen dersom studiegruppen er homogen.1
• Matching
Matching innebærer å velge kontroller slik at fordelingen av potensielle confounders (f. eks alder eller røykestatus) er så lik som mulig som blant tilfellene. I praksis brukes dette kun i case-control studier, men det kan gjøres på to måter:
- Parmatching-valg av for hver sak en eller flere kontroller med lignende egenskaper (f. eks. Frekvens matching-sikre at som en gruppe tilfellene har lignende egenskaper til kontrollene
Oppdage og kontrollere for confounding på analysetrinnet
tilstedeværelsen eller omfanget av confounding i epidemiologiske studier er evaluert ved å observere graden av avvik mellom råolje estimat (uten å kontrollere for confounding) og justert estimat etter regnskap for potensielle confounder (s). Hvis estimatet har endret seg og det er liten variasjon mellom stratumspesifikke forholdstall( se nedenfor), så er det tegn på confounding.
det er upassende å bruke statistiske tester for å vurdere tilstedeværelsen av confounding, men følgende metoder kan brukes for å minimere effekten.
• Stratifisering
Stratifisering gjør det mulig å undersøke sammenhengen mellom eksponering og utfall innenfor ulike lag av den konfunderende variabelen, for eksempel etter alder eller kjønn. Styrken til foreningen måles i utgangspunktet separat innenfor hvert lag av den konfunderende variabelen. Forutsatt at stratumspesifikke priser er relativt ensartede, kan de deretter samles for å gi et sammendragsestimat som justert eller kontrollert for potensiell confounder. Et eksempel er Mantel-Haenszel-metoden. En ulempe ved denne metoden er at jo mer den opprinnelige prøven er stratifisert, desto mindre blir hvert lag, og kraften til å oppdage foreninger reduseres.
• Multivariabel analyse
Statistisk modellering (f. eks. multivariabel regresjonsanalyse) brukes til å kontrollere for mer enn en confounder samtidig, og muliggjør tolkning av effekten av hver confounder individuelt. Det er den mest brukte metoden for å håndtere confounding på analysefasen.
• Standardisering
Standardisering står for konfounders (generelt alder og kjønn) ved å bruke en standard referansepopulasjon for å negere effekten av forskjeller i fordelingen av konfunderende faktorer mellom studiepopulasjoner. Se «Tellere, denominatorer og populasjoner i fare» for mer informasjon.
Residual confounding
det er bare mulig å kontrollere for confounders på analysetrinnet hvis data på confounders ble nøyaktig samlet inn. Residual confounding oppstår når alle confounders ikke er tilstrekkelig justert for, enten fordi de har blitt feilaktig målt, eller fordi de ikke har blitt målt (for eksempel ukjente confounders). Et eksempel ville være sosioøkonomisk status, fordi det påvirker flere helseutfall, men er vanskelig å måle nøyaktig.3
Interaksjon (effektmodifisering)
Interaksjon oppstår når retningen eller størrelsen på en sammenheng mellom to variabler varierer i henhold til nivået av en tredje variabel (effektmodifikatoren). For eksempel kan aspirin brukes til å håndtere symptomene på virussykdommer, som influensa. Imidlertid, mens det kan være effektivt hos voksne, er aspirinbruk hos barn med virussykdommer forbundet med leverdysfunksjon og hjerneskade (Reyes syndrom).4 i dette tilfellet endres effekten av aspirin på å håndtere virussykdommer etter alder.
der det finnes interaksjon, kan det være misvisende å beregne et samlet estimat av en assosiasjon. I motsetning til confounding er interaksjon et biologisk fenomen og bør ikke statistisk justeres for. En vanlig metode for å håndtere samhandling er å analysere og presentere assosiasjonene for hvert nivå av den tredje variabelen. I eksemplet ovenfor vil oddsene for å utvikle Reyes syndrom etter aspirinbruk i virussykdommer være langt større hos barn sammenlignet med voksne, og dette vil markere alderens rolle som en effektmodifikator. Interaksjon kan bekreftes statistisk, for eksempel ved hjelp av en kjikvadrert test for å vurdere for heterogenitet i stratum-spesifikke estimater. Imidlertid er slike tester kjent for å ha lav effekt for å oppdage interaksjon5, og en visuell inspeksjon av stratumspesifikke estimater anbefales også.
- Hennekens CH, Buring JE. Epidemiologi I Medisin, Lippincott Williams & Wilkins, 1987.
- Carneiro I, Howard N. Introduksjon Til Epidemiologi. Open University Press, 2011.
- http://www.edmundjessop.org.uk/fulltext.doc – Tilgjengelig 20/02/16
- McGovern MC. Reyes syndrom og aspirin: la oss ikke glemme. BMJ 2001; 322:1591.
- Marshall SW. Strøm for tester av interaksjon: effekt av å øke type 1 feilrate. Epidemiologiske perspektiver og innovasjoner 2007; 4: 4.
Leave a Reply