15.3:물리적 특성의 카르복시산
학습 목표
- 을 비교를 끓는점의 카르복시산과 알코올의 비슷한 몰 질량.
- 물 중 카르 복실 산의 가용성과 물 중 비교 가능한 알칸 및 알콜의 가용성을 비교하십시오.
많은 카르 복실 산은 불일치하는 냄새가 나는 무색의 액체입니다. 5~10 개의 탄소 원자를 가진 카르 복실 산은 모두”goaty”냄새를 가지고 있습니다(Limburger 치즈의 냄새를 설명합니다). 이 산은 또한 생산 활동에 의하여 피부의 박테리아에서 인간 피지(오일 피부),에 대하여 설명하는 냄새의 환기가 잘 탈의실이 있습니다. 탄소 원자가 10 개 이상인 산은 왁스 같은 고체이며,그 냄새는 몰 질량이 증가하고 결과적으로 휘발성이 감소함에 따라 감소합니다.
카르 복실 산은 분자 사이에 강한 수소 결합을 나타낸다. 따라서 그들은 비교 가능한 몰 질량의 다른 물질에 비해 높은 비등점을 갖는다.
카르복실기는 물 분자와의 수소 결합에 쉽게 관여한다(그림\(\PageIndex{1}\)). 1~4 개의 탄소 원자를 갖는 산은 물과는 완전히 혼화 가능하다. 쌍극자 힘이 덜 중요 해지고 분산력이 더 우세 해지기 때문에 탄소 사슬 길이가 증가함에 따라 용해도가 감소합니다. 헥산 산은 물(약 1.0g/100g 의 물)에 거의 용해되지 않습니다. 큰 비극성 탄화수소 성분을 가진 팔미틴산은 본질적으로 물에는 불용성이다. 카르 복실 산은 일반적으로 에탄올,톨루엔 및 디 에틸 에테르와 같은 유기 용매에 용해된다.
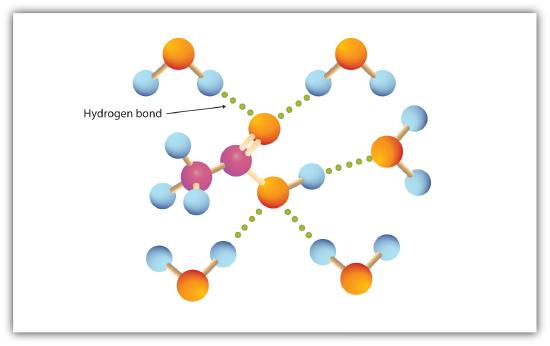
표 15.4.1 은 선택된 카르 복실 산에 대한 몇 가지 물리적 특성을 나열합니다. 처음 6 개는 동족체입니다. 끓는점은 몰 질량이 증가함에 따라 증가하지만 융점은 규칙적인 패턴을 보이지 않는다는 것을 알 수 있습니다.나는 이것이 어떻게 작동하는지 잘 모르겠습니다.: Physical Constants of Carboxylic Acids
Concept Review Exercises
- Which compound has the higher boiling point—butanoic acid (molar mass 88) or 2-pentanone (molar mass 86)? Explain.
- Would you expect butyric acid (butanoic acid) to be more or less soluble than 1-butanol in water? Explain.
답변
- 부티르산의 수소 결합(이 없 intermolecular 수소 결합에서 2-pentanone.)
- 더 많은 수용성이 있기 때문에 더 많은 다양한 수소 결합
키 테이크 아웃
- 카르복시산 높은 끓는 점에 비해 다른 물질의 비교 분자량. 비등점은 몰 질량과 함께 증가합니다.
- 1~4 개의 탄소 원자를 갖는 카르 복실 산은 물과는 완전히 혼화 가능하다. 용해도는 몰 질량에 따라 감소합니다.
운동
-
어느 화합물이 더 높은 끓는점을 가지는가-CH3CH2CH2OCH2CH3 또는 CH3CH2CH2COOH? 설명한다.
-
어느 화합물이 더 높은 끓는점을 가지는가-CH3CH2CH2CH2CH2OH 또는 CH3CH2CH2COOH? 설명한다.
-
어떤 화합물이 물—CH3COOH 또는 CH3CH2CH2CH3 에 더 용해됩니까? 설명한다.
-
어느 화합물이 물—CH3CH2COOH 또는 CH3CH2CH2CH2CH2COOH 에 더 용해됩니까? 설명한다.
답변
-
CH3CH2CH2COOH 때문에 수소 결합(이 없 intermolecular 수소 결합으로 CH3CH2CH2OCH2CH3.)
-
CH3COOH 종사하기 때문에서는 수소와 결합 물(이 없 intermolecular 수소 결합으로 CH3CH2CH2CH3.)
Leave a Reply