2019 Gina-retningslinjerne for astmabehandling hos voksne
US Pharm. 2020;45(7/8):18-24.
abstrakt: etablering af astmasymptomkontrol ved hjælp af farmakologiske og ikke-farmakologiske interventioner forbedrer livskvaliteten og forhindrer eksacerbationer hos patienter med astma. Global Initiative for astma 2019 retningslinjer giver anbefalinger til astmabehandling organiseret i fem trin, der korrelerer med sygdommens sværhedsgrad. Medicinske muligheder inkluderer inhalerede kortikosteroider (ICS), langtidsvirkende beta2-agonister, kortvirkende beta2-agonister (SABAs), leukotrien-receptorantagonister og orale kortikosteroider. Nylige data viser ugunstige resultater for SABAs, der anvendes alene til efter behov behandling af symptomer på mild astma. Retningslinjeændringer inkluderer anvendelse af en lavdosis ICS med formoterol til efter behov behandling hos voksne med mild astma eller til brug, når en SABA ville blive brugt. Passende, effektive medicinregimer kombineret med rådgivning om korrekt inhalatorteknik hjælper patienter med at nå astmastyringsmål.
astma, en kronisk inflammatorisk luftvejssygdom, der er kendetegnet ved luftvejshyperresponsivitet, kan have symptomer som vejrtrækning, åndenød, tæthed i brystet og hoste.1 Disse symptomer kan variere over tid og i intensitet, hvilket gør effektiv behandling af astma vigtig. Symptomudløsere kan omfatte motion, virale luftvejsinfektioner og miljømæssige faktorer, såsom rygning. Symptomer, der ikke behandles, kan føre til forværringer. En forværring er en akut episode, hvor symptomerne forværres drastisk, og lungefunktionen gradvist falder. Enhver forekomst af en forværring berettiger en diskussion om patientens nuværende astmabehandlingsregime på grund af risikoen for indlæggelse, akutbesøg og astmarelateret død.
2019 Global Initiative for astma (GINA) retningslinjer anbefaler ikke brug af en kortvirkende beta2-agonist (SABA) inhalator alene til behandling af mild astma; i stedet anbefaler de lavdosis inhaleret kortikosteroid (ICS) – formoterol brug efter behov og til vedligeholdelsesbehandling.2 hos patienter, der har svær eller svær at behandle astma, kan andre muligheder betragtes som tilføjelser til inhalatorbehandling, såsom leukotrien-receptorantagonister (ltras), tiotropium, biologiske lægemidler og orale kortikosteroider (OCS).
astmakontrol angiver, i hvilket omfang astmafunktioner kan observeres hos patienten eller er blevet reduceret eller elimineret ved behandling.2 astmakontrol bør gennemgås i løbet af de foregående 4 uger. Patienten skal stilles følgende spørgsmål: “i de foregående 4 uger har du haft: 1) astmasymptomer på dagen mere end to gange om ugen? 2) eventuelle natlige vækkelser på grund af astma? 3) at bruge en astma reliever for symptomer mere end to gange om ugen? 4) eventuelle aktivitetsbegrænsninger på grund af astma?”Hvis patienten svarer” nej ” på alle fire spørgsmål, er hans eller hendes astma godt kontrolleret. Hvis patienten svarer ” ja “på et eller to af spørgsmålene, kontrolleres astmaen delvist, men hvis svaret er” ja ” til tre til fire af spørgsmålene, kontrolleres astmaen ikke godt.2 risikofaktorer, der kan forårsage en forværring, inkluderer ukontrolleret astma, rygning, allergeneksponering, luftforurening, comorbiditeter såsom fedme og høj SABA-brug.
vurdering af overholdelse af patientens inhalerede medicin er et andet vigtigt skridt. Der er mange grunde til, at en patient muligvis ikke overholder astmamedicin, herunder vanskeligheder med at bruge inhalatorudstyr, medicinomkostninger, glemsomhed, manglende forståelse af de foreskrevne anvisninger og opfattelse af, at medicinen ikke er nødvendig.2
håndtering og behandling
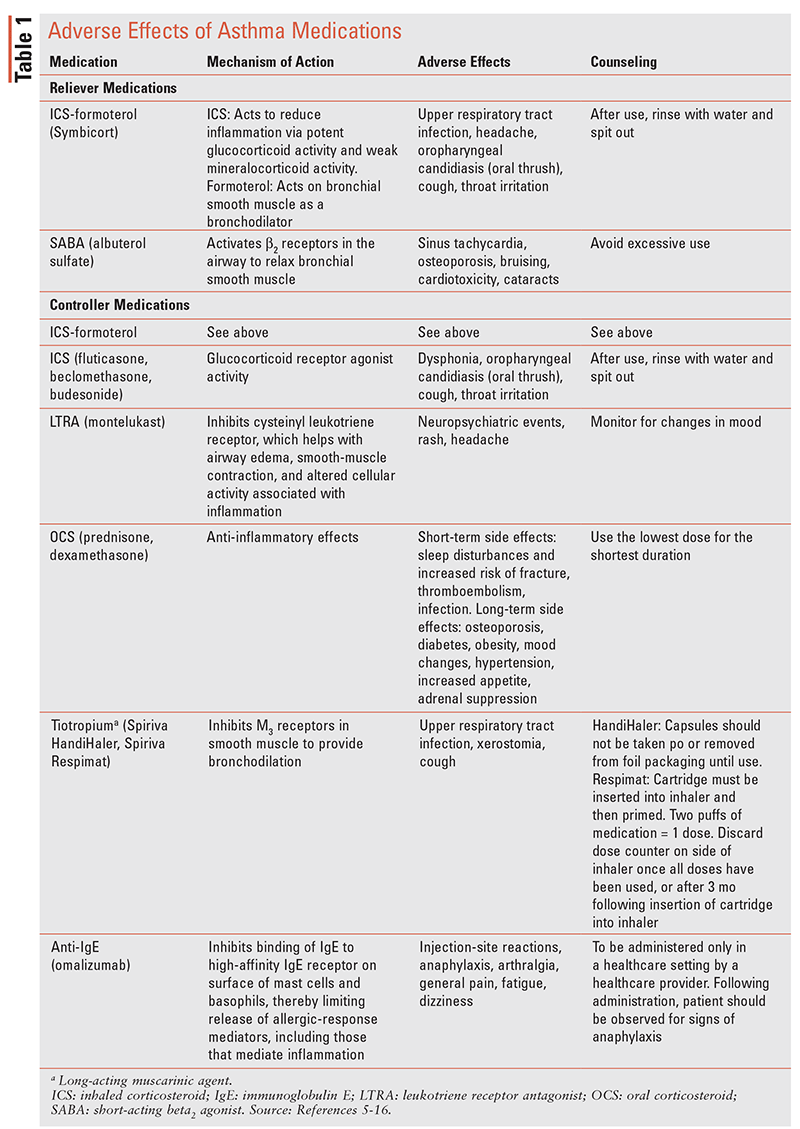
mål for terapi for astma inkluderer opnåelse af kontrol af symptomer for at opretholde normale aktivitetsniveauer, forebyggelse af vedvarende luftstrømsbegrænsning og reduktion af bivirkninger af medicin, der er diskuteret i tabel 1. Farmakologiske og ikke-farmakologiske interventioner reducerer risikoen for fremtidige forværringer, der fører til indlæggelse eller astma-relateret død.2
Nonpharmacologic Management
Nonpharmacologic interventioner for alle astmapatienter omfatter åndedrætsøvelser, øget fysisk aktivitet, inkorporering af en sund kost og undgåelse af eksponering for røg og andre stoffer.2 praksis med yoga og vejrtrækningsmetoder som Buteyko og Paporth teknikker ændrer vejrtrækningsmønstre for at reducere hyperventilation og derved fremme frivillig reduktion i reliever brug og forbedring af astmasymptomer.3 hos overvægtige patienter er vægttab kombineret med aerob-og styrkeøvelser to gange ugentligt mere effektivt end fysisk aktivitet alene til symptomkontrol.2 rådgivning om korrekt inhalatorteknik hjælper patienter med at nå astmastyringsmål.
farmakologisk behandling
der foretages justeringer af astmamedicinske regimer gennem den kontrolbaserede astmastyringscyklus, der er afbildet i figur 1.2
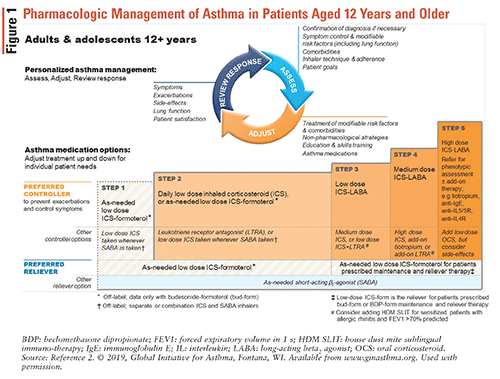
Når en diagnose af astma er stillet, bør en ICS-indeholdende controller-behandling påbegyndes på grund af den større forbedring i lungefunktionen, end når ICS-controller-behandling ikke anvendes. Dette er en vigtig ændring i Gina-retningslinjerne for 2019, da det tidligere blev anbefalet at give nydiagnosticerede patienter en SABA alene. ICS-formoterol kombinationsinhalatoren er den foretrukne efter behov reliever terapi uanset astma sværhedsgrad. Den alternative reliever terapi er en SABA; det skal dog parres med en anden inhalator, der indeholder ICS. ICS-formoterol inhalatorer er sikre og effektive, og deres evne til at blive brugt både efter behov og til vedligeholdelsesbehandling gør dem nemme for patienterne at bruge.2
GINA anbefaler følgende astmabehandling trin2:
• Trin 1: Dette trin anbefales til patienter med mild astma, der har symptomer mindre end to gange om måneden og ingen risiko for eksacerbationer. Som tidligere nævnt, baseret på nye beviser, anbefaler Gina-retningslinjerne fra 2019 ikke længere SABA-brug alene til behandling af astma.
• Trin 2: Det foretrukne regulatorregime er efter behov lavdosis ICS-formoterol eller daglig lavdosis ICS plus SABA efter behov. ICS-formoterol-regimet undgår behovet for daglige ICS, samtidig med at det giver lignende fordele for træningsinduceret bronchokonstriktion som daglige ICS med efter behov SABA.
• Trin 3: Foretrukne controllerbehandlinger inkluderer en lavdosis ICS-langtidsvirkende beta2–agonist (LABA) plus efter behov SABA eller lavdosis ICS-formoterol til både vedligeholdelses-og relieverbehandling.
• Trin 4: Den foretrukne controller-behandling er lavdosis ICS-formoterol som vedligeholdelses-og relieverbehandling eller mellemdosis ICS-LABA som vedligeholdelse plus SABA efter behov. Bemærk, at ICS-formoterol ikke bør kombineres med en ICS-LABA indeholdende en anden LABA.
• Trin 5: vedvarende eksacerbationer eller symptomforværring forekommer på trods af vedhæftning og korrekt inhalatorteknik. Disse patienter anses for at have svær eller svær at behandle astma og bør henvises til en pulmonologist.
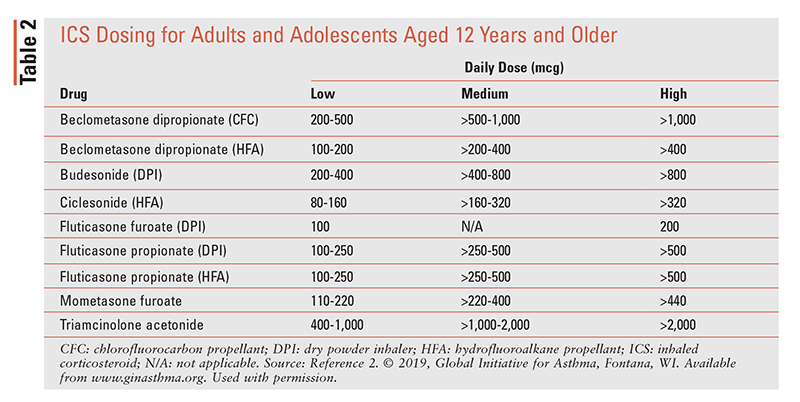
det er hensigtsmæssigt at optrappe de trin, der er skitseret ovenfor, når patienter har vedvarende dårlig symptomkontrol eller eksacerbationer på trods af lavdosis ICS-behandling i 2 til 3 måneder. Det er hensigtsmæssigt at træde ned, når patienten har god symptomkontrol og stabil lungefunktion i mindst 3 måneder. Valgmulighederne for at træde ned afhænger af, hvilken medicin patienten tager, og hvilket skridt patienten er på, men for de fleste patienter er resultatet værre, hvis ICS eller LABA stoppes fuldstændigt.2 ICS dosering er beskrevet i tabel 2.
symptomer kan vurderes med værktøjer som Astmakontrolspørgeskemaet, Astmakontroltesten og Royal College of Physicians’ tre spørgsmål.2 disse spørgeskemaer gør det muligt for en score at blive forbundet med symptomer og spørge patienter om hyppigheden og typerne af symptomer, såsom opvågninger om natten og begrænsninger i daglige aktiviteter.
eksacerbationer
udtrykket astmaforværring henviser til den akutte forværring af lungefunktion og symptomer ud over, hvad patienten normalt oplever. Den foretrukne relieverbehandling under en eksacerbation er lavdosis ICS-formoterol, der kan øges efter behov, når symptomerne forværres. Brug af en ICS-LABA (beclomethason eller budesonid og formoterol) som både reliever og controller medicin forbedrer symptomkontrol og reducerer indlæggelser og OCS brug sammenlignet med den samme eller højere dosis af en controller plus efter behov SABA.4
et kort OCS-kursus er en behandlingsmulighed under en forværring, når patienten ikke reagerer på en øget dosis af reliever og controller efter 2 til 3 dage, har en historie med pludselige alvorlige forværringer eller har hurtigt forværret lungefunktion (maksimal ekspiratorisk strømning eller tvungen ekspiratorisk volumen i 1 sekund <60% af personlig bedste eller forudsagt værdi).4
bivirkninger af astmamedicin
se tabel 1 for en oversigt over bivirkninger af forskellige astmamedicin.5-16
svær eller svær at behandle astma
svær eller svær at behandle astma refererer til ukontrolleret astma i behandlingstrin 4 og 5 på trods af tilstrækkelig overholdelse af behandling og behandling af medvirkende faktorer. Efter indledende vurdering skiftes patienter i alderen 12 år og ældre med utilstrækkeligt kontrolleret astma, der tager en MIDDELDOSIS ICS plus en LABA og/eller en tredje controller, såsom ltra eller vedvarende frigivelse theophyllin, til et forsøg med en højdosis ICS i 3 til 6 måneder. Ud over at øge ICS, et forsøg med en add-on nonbiologic såsom tiotropium, en leukotrien modifier, eller OCS kan overvejes. For voksne patienter, der har vedvarende astmasymptomer på trods af moderat dosis eller højdosis ICS og LABA, anbefaler Gina-retningslinjerne fra 2019 som en tilføjelse.17
Hvis nonbiologics såsom LABA, tiotropium og leukotrien modifikatorer ikke klarer en patients astmasymptomer, kan biologics overvejes afhængigt af prisen og patientens ressourcer. Anti-immunoglobulin E-behandling, såsom omalisumab, kan overvejes hos patienter med allergisk astma. I tilfælde af at biologiske lægemidler ikke er en mulighed for en patient, kan en OCS i en dosis på 7, 5 mg eller mindre pr. Imidlertid er OCS forbundet med betydelige bivirkninger, såsom osteoporose, fedme, diabetes, grå stær, hypertension og binyrebarksuppression, og bør derfor betragtes som sidste linje.17
studier
et dobbeltblindt forsøg udført af O ‘ Byrne og kolleger undersøgte fordelen ved at bruge en ICS plus en SABA sammenlignet med konventionel behandling.18 i alt 3.849 patienter i alderen 12 år eller derover med mild astma blev tilfældigt tildelt terbutalin (to gange daglig placebo plus terbutalin 0,5 mg prn), budesonid-formoterol (to gange daglig placebo plus budesonid-formoterol 200 mcg/6 mcg prn) eller budesonidvedligeholdelse (to gange daglig budesonid 200 mcg plus terbutalin prn). Det primære mål var at afgøre, om budesonid-formoterol efter behov var bedre end efter behov terbutalin til symptomkontrol. Dette resultat blev målt via data opnået fra en elektronisk symptomdagbog.
efter behov budesonid-formoterol var overlegen med hensyn til astma-symptomkontrol sammenlignet med efter behov terbutalin hos patienter med mild astma. Budesonid-formoterolpatienter viste velkontrolleret astma i 34,4% af ugerne versus 31,1% af ugerne i terbutalingruppen (P = .046). Terbutalin var forbundet med den højeste årlige forekomst af alvorlige eksacerbationer (0.20) sammenlignet med budesonid-formoterol (0,07) og budesonidvedligeholdelse (0,09). En fordel ved brug af budesonid-formoterol var, at eksponeringen for kortikosteroider blev reduceret på grund af den 17% lavere budesoniddosis i denne gruppe sammenlignet med budesonidvedligeholdelsesgruppen (henholdsvis 57 mcg vs. 340 mcg).18
Bateman og kolleger undersøgte effektiviteten af en inhaleret glukokortikoidkomponent med en hurtigtvirkende reliever til mild astma.5 Dette 52-ugers dobbeltblinde multicenterstudie omfattede 4.215 patienter med mild astma i alderen 12 år og derover, som var berettiget til behandling med regelmæssige inhalerede glukokortikoider. Deltagerne blev opdelt i to grupper for at vurdere, om budesonid-formoterol eller budesonid vedligeholdelsesbehandling to gange dagligt havde bedre effekt med hensyn til årlige satser for alvorlige eksacerbationer. Budesonid-formoterolgruppen var ikke ringere end budesonid-vedligeholdelsesgruppen for alvorlige eksacerbationer. Derudover var den mediane daglige afmålte dosis inhaleret glukokortikoid lavere i budesonid-formoterolgruppen (66 mcg) end i budesonid-vedligeholdelsesgruppen (267 mcg). Tiden til første eksacerbation var ens mellem grupperne; der var imidlertid en forskel på 0,11 U til fordel for budesonid-vedligeholdelsesgruppen, som havde lavere score på Astmakontrolspørgeskemaet-5 (ACK-5) sammenlignet med budesonid-formoterol-gruppen. Den minimale klinisk vigtige forskel i ACK – 5 score er 0,5 U. Derudover var der ingen forskel i bivirkninger, astmarelaterede seponeringer eller dødelighed mellem de to grupper. Denne undersøgelse og O ‘ Byrne-undersøgelsen understøtter den nuværende Gina-anbefaling fra 2019 mod brugen af en SABA alene og til brug af ICS-formoterol i stedet.
en undersøgelse foretaget af Gibson og kolleger undersøgte effekten og sikkerheden af oral acithromycin som tillægsbehandling hos patienter med ukontrolleret vedvarende astma, der også tog en MIDDELDOSIS eller højdosis ICS plus en LABA.17 i dette randomiserede, dobbeltblinde, placebokontrollerede forsøg med parallelgruppe blev 420 patienter tilfældigt tildelt en af to behandlingsgrupper (500 mg eller placebo tre gange om ugen i 48 uger). De primære effektendepunkter omfattede hyppighed af total (svær og moderat) astmaforværring og samlet astmarelateret livskvalitet i undersøgelsesperioden.44% af patienterne oplevede mindst en eksacerbation sammenlignet med 61% af placebopatienterne (P <.0001). Derudover gav brug af astmarelateret livskvalitet signifikant fordel, betegnet ved forbedring i alle kategorier af vurderingsskalaen (dvs.aktivitet, symptom, følelser og miljømæssige domæner) for astmarelateret livskvalitet. Den eneste anden bemærkelsesværdige forskel mellem studiegrupperne var forekomsten af diarre, som var signifikant højere hos patienter med acithromycin (34% vs. 19% af placebopatienterne). Til sikkerhedsovervågning blev EKG ‘ er udført ved screening efter 6 ugers behandling og ved afslutningen af behandlingen. 480 ms resulterede i tilbagetrækning fra studiet hos to patienter (en fra hver gruppe).17
ændringer i retningslinjerne for 2019
retningslinjerne for 2019 inkluderer fem bemærkelsesværdige ændringer med hensyn til astmabehandling hos voksne. Den første ændring er overgangen fra SABA-kun behandling til ICS-indeholdende behandling til efter behov behandling af symptomer ved mild astma.4 den anden ændring er brugen af tillægsbehandling med lav dosis tre gange om ugen til langtidsbehandling af patienter med symptomatisk astma på trods af ICS-LABA-behandling med moderat dosis eller høj dosis; potentielle bivirkninger bør dog overvejes.17
den tredje ændring er anbefalingen for dupilumab, et anti–interleukin-4-receptor alfa monoklonalt antistof, som en yderligere behandlingsmulighed for patienter i alderen 12 år og ældre med svær type 2-astma eller OCS-afhængig astma.19 et forsøg udført af dupilumab og kolleger viste, at dupilumab øgede lungefunktionen og reducerede alvorlige eksacerbationer hos patienter med ukontrolleret vedvarende astma.20
den fjerde ændring er kun at inkludere højdosis ICS-LABA-behandling i trin 5, mens den tidligere var inkluderet i trin 4 med moderat dosis ICS-LABA; dette skyldes anbefalingen om, at ICS med høj dosis kun skal ordineres i et par måneder baseret på overvejelse af tilknyttede bivirkninger.17 den femte ændring er skiftet af vedligeholdelse OCS fra en” foretrukken “behandlingsmulighed til” anden controller option ” i trin 5, baseret på den høje risiko for negative resultater.19
konklusion
baseret på nye data anbefaler de opdaterede Gina-retningslinjer for 2019 ikke brug af en SABA-inhalator alene til behandling af mild astma; i stedet anbefales lavdosis ICS-formoterol til efter behov og vedligeholdelsesbehandling. For patienter, der har svær eller svær at behandle astma, kan andre muligheder betragtes som tillægsbehandling til inhalatorbehandling, herunder LTRA, tiotropium, biologics, asithromycin og OCS. For at sikre bedre overholdelse af medicin, astma terapiregimer bør være patientspecifikke, med en trinvis tilgang taget for at finde et regime, der styrer patientens astmasymptomer, mens patienten holdes på den lavest mulige dosis, og bør også være omkostningseffektiv.
1. Astma og Allergi Foundation of America. Astmaanfald. www.aafa.org/asthma-symptoms. adgang til 8. April 2020.
2 . Globalt initiativ til astma. Global strategi for astmastyring og forebyggelse, 2019. www.ginasthma.org. adgang til 8. April 2020.
3. Santino TA, Chaves GS, Freitas DA, et al. Åndedrætsøvelser til voksne med astma. Cochrane Database Syst Rev. 2020; 3 (3):CD001277.
4. O ‘ Byrne PM, Fitsgerald JM, Bateman ED, et al. Inhaleret kombineret budesonid-formoterol efter behov i mild astma. N Engl J Med. 2018;378(20):1865-1876.
5. Bateman ED, Reddel HK, O ‘ Byrne PM, et al. Efter behov budesonid-formoterol versus vedligeholdelse budesonid i mild astma. N Engl J Med. 2018;378(20):1877-1887.
6. Symbicort (budesonide-formoterol) indlægsseddel. Wilmington, DE: AstraZeneca Lægemidler LP, januar 2017.
7. Reed CE. Astma hos ældre: diagnose og behandling. J Allergi Clin Immunol. 2010;126(4):681-687.
8. Proair HFA (albuterol) indlægsseddel. Teva respiratorisk, LLC; februar 2019.
9. Flovent HFA (fluticasone) indlægsseddel. Forskning Triangle Park, NC:
10. Singulair (montelukast) indlægsseddel. Hvidhus Station, NJ: Merck & Co, Inc; April 2020.
11. Lin P, et al. Kortvarig brug af orale kortikosteroider og relaterede skader blandt voksne i USA: populationsbaseret kohortestudie. BMJ. 2017; 357: j1415.
12. Foster JM, McDonald VM, m Guo, Reddel HK. “Jeg har mistet i alle aspekter af mit liv”: den skjulte byrde ved svær astma. EUR Respir J. 2017;50(3):1700765.
13. Rayos (prednison) indlægsseddel. Deerfield, IL: horisont Pharma, Inc; 2012.
14. Spiriva HandiHaler (tiotropium) indlægsseddel. Ridgefield, CT: Boehringer Ingelheim Pharmaceuticals, Inc; februar 2018.
15. Spiriva Respimat (tiotropium) indlægsseddel. Ridgefield, CT: Boehringer Ingelheim Pharmaceuticals, Inc; marts 2019.
16. Indlægsseddel. South San Francisco, CA: Genentech, Inc; maj 2019.
17. Gibson PG, Yang IA, Upham JV, et al. En randomiseret, dobbeltblind, placebokontrolleret undersøgelse. Lancet. 2017;390(10095):659-668.
18. O ‘ Byrne PM, Barnes PJ, Rodrigues-Roisin R, et al. Lavdosis inhaleret budesonid og formoterol ved mild vedvarende astma: OPTIMA randomiseret forsøg. Am J Respir Crit Pleje Med. 2001;164(8):1392-1397.
19. Castro M, Corren J, Pavord ID, et al. Dupilumab virkning og sikkerhed ved moderat til svær ukontrolleret astma. N Engl J Med. 2018;378(26):2486-2496.
20. S, Castro M, Corren J, et al. Dupilumab effekt og sikkerhed hos voksne med ukontrolleret vedvarende astma trods brug af inhalerede kortikosteroider med middel til høj dosis plus en langtidsvirkende beta2-agonist: et randomiseret dobbeltblindet placebokontrolleret pivotalt fase 2B-dosisintervallet studie. Lancet. 2016;388(10039):31-44.
Indholdet i denne artikel er kun til orientering. Indholdet er ikke beregnet til at erstatte professionel rådgivning. Afhængighed af oplysninger i denne artikel er udelukkende på egen risiko.
Leave a Reply