3D Bioprinting af levende væv
3D-trykte tykke vaskulariserede vævskonstruktioner til organteknik og regenerativ medicin
fremskridt inden for lægemiddelprøvning og regenerativ medicin kunne i høj grad drage fordel af laboratoriekonstrueret humant væv bygget af en række celletyper med præcis 3d-arkitektur. Men produktionen af større end millimeter store humane væv har været begrænset af mangel på metoder til opbygning af væv med indlejrede livsbærende vaskulære netværk.
tværfaglig forskning har ført til udviklingen af en multi-materiale 3D bioprinting metode, der genererer vaskulariseret væv sammensat af levende humane celler, der er næsten ti gange tykkere end tidligere manipuleret væv, og som kan opretholde deres arkitektur og funktion i op til seks uger. Metoden bruger en tilpasselig, trykt silikoneform til at huse og lodde det trykte væv på en chip. Inde i denne form udskrives et gitter med større vaskulære kanaler, der indeholder levende endotelceller i silikoneblæk, hvori et selvbærende blæk indeholdende levende mesenkymale stamceller (MSC ‘ er) er lagdelt i et separat udskriftsjob. Efter udskrivning anvendes en væske sammensat af fibroblaster og ekstracellulær matrice til at fylde åbne områder inden for konstruktionen, idet der tilsættes en bindevævskomponent, som tværbinder og yderligere stabiliserer hele strukturen.
den resulterende bløde vævsstruktur kan straks perfunderes med næringsstoffer såvel som vækst-og differentieringsfaktorer via et enkelt indløb og udløb i modsatte ender af chippen, der forbinder til den vaskulære kanal for at sikre overlevelse og modning af cellerne. I en proof-of-principle-undersøgelse tillod en centimeter tykke bioprintede vævskonstruktioner indeholdende humane knoglemarv MSC ‘ er omgivet af bindevæv og understøttet af en kunstig endotelforet vaskulatur cirkulation af knoglevækstfaktorer og efterfølgende induktion af knogleudvikling.
denne innovative bioprinting tilgang kan ændres for at skabe forskellige vaskulariserede 3D væv til regenerativ medicin og lægemiddelprøvning bestræbelser. Vi undersøger også brugen af 3D-bioprinting til at fremstille nye versioner af instituttets organer på chipsenheder, hvilket gør deres fremstillingsproces mere automatiseret og muliggør udvikling af stadig mere komplekse mikrofysiologiske enheder. Denne indsats har resulteret i det første helt 3D-trykte orgel på en chip – et hjerte på en chip – med integrerede bløde belastningssensorer.
-
 3D Bioprinting af levende væv
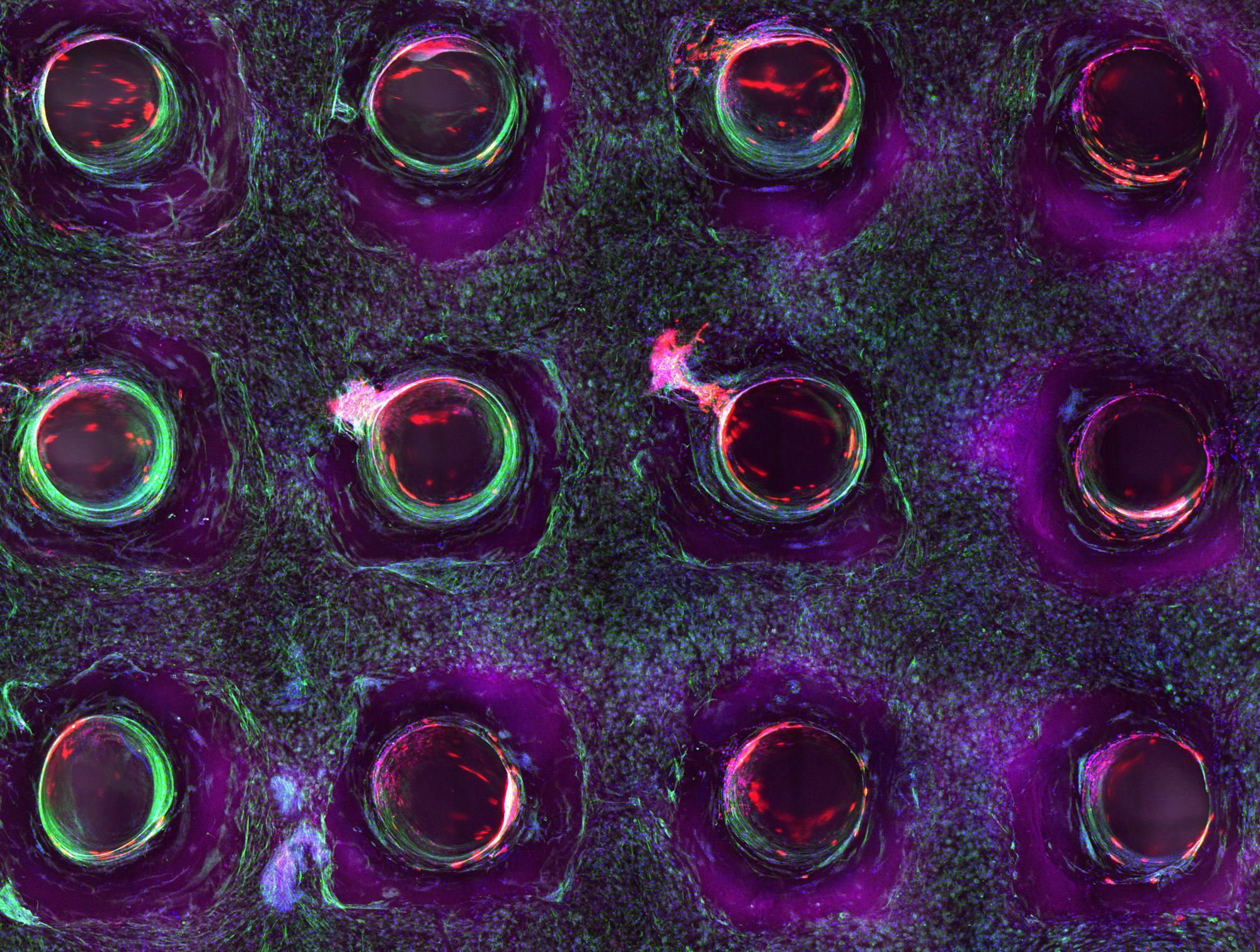
3D Bioprinting af levende væv1/7 tværsnit af langvarig perfusion af HUVEC-foret (rød) vaskulære netværk understøtter hndfladen(grøn) matrice. 3D Bioprinting af levende væv2/7 ovenfra og ned visning af langvarig perfusion af huvec-foret (rødt) vaskulært netværk, der understøtter hndfladen (grøn) matrice. 3D Bioprinting af levende væv3/7 Fotografi tværsnit af trykt vævskonstruktion opstaldet i en perfusion kammer. 
4/7 Fotografi tværsnit af trykt vævskonstruktion, der er anbragt i en perfusion kammer. 
5/7 Photograph of a printed tissue construct housed within a perfusion chamber. 6/7 Photograph of vasculature network and cell inks. 
7/7 Photograph of 3D printed vasculature network (red) within Red is the - Prev

Leave a Reply