Lavalamper
Hvad synes du om, når du hører ordet “groovy”? Bell bund bukser? Blomster? Hvad med lavalamper?
lavalamper var meget populære tilbage i de groovy 1960 ‘ ere! Mange mennesker har dem stadig hjemme i dag.
de fleste lamper lyser op i et rum. Men lavalamper er hovedsageligt bare sjove at se på. De har farvede vokskugler, der flyder rundt i en gennemsigtig væske.
vidste du det?Edvard Craven har designet lavalampen. Han baserede det på en ægtimer, han så på en pub! Ægget timeren havde en kugle af voks suspenderet i vand. Da voksen smeltede, var ægget klar til at spise.
lavalamper er også en “groovy” måde at se fysik og kemi principper i aktion.

Hvad er den kinetiske molekylære teori?
for at forstå, hvordan lavalamper fungerer, skal du forstå kinetisk molekylær teori. Det hedder, at alt stof består af molekyler, der altid bevæger sig. Disse molekyler har kinetisk energi. Mængden af energi afhænger af temperaturen. Når det er varmere, har molekyler mere energi. Og når de har mere energi, bevæger de sig hurtigere. Der er tre mest almindelige tilstande af materie.
molekylerne i faste stoffer har mindst energi. Det betyder, at de bevæger sig langsommere end molekyler i væsker og gasser.
molekylerne i gasser har mest energi af alle. De bevæger sig hurtigst.
Hvordan er kinetisk energi relateret til densitet?
kinetisk molekylær teori kan hjælpe dig med at forstå tæthed. Tæthed refererer til, hvor meget stof der er i et givet rumfang.
har du nogensinde kastet en mønt i en springvand eller en sten i en dam? Du har sikkert bemærket, at disse genstande synker i vand. Og du har sikkert bemærket, at andre genstande, som kviste, flyder på vand. De objekter, der er tættere end vand synke. Og de genstande, der er mindre tætte end vand, flyder.
men hvad har dette at gøre med lavalamper? Husk kuglerne-lad os kalde dem “globs” for kort – der flyder rundt? Ved stuetemperatur er Globerne lidt tættere end den omgivende væske. Derfor sidder de i bunden af lampen. Men når du tænder lampen, bliver Globerne varme op. Molekylerne bevæger sig hurtigere. Globerne bliver mindre tætte end den omgivende væske. De rejser sig og begynder at flyde rundt!
vidste du det?
varmluftsballoner fungerer på samme måde som Globerne i lavalampen.
Hvordan påvirker evnen til at blande, hvordan en lavalampe fungerer?

så hvorfor blandes ikke vokskloderne i en lavalampe med den omgivende væske?
tænk på chokoladesirup og mælk. De er blandbare væsker. Det betyder, at de kan blandes for at danne en homogen blanding. Chokoladesirupen blandes fuldstændigt med mælken for at danne lækker chokolademælk!
men nogle væsker er ublandbare. De blander sig ikke med hinanden. Det hele afhænger af tiltrækningskraften mellem molekylerne i de to væsker.
Hvad sker der for eksempel, når du prøver at blande olie og eddike – som i en salatdressing? Molekylerne i eddike er mere tiltrukket af hinanden end til molekylerne i olie. Molekylerne i olie er mere tiltrukket af hinanden end af molekylerne i eddike. Uanset hvor meget du ryster eller rører din dressing, forbliver de aldrig blandet sammen.
men chokoladesirupmolekyler tiltrækkes af mælkemolekyler. Og mælkemolekyler tiltrækkes af chokoladesirupmolekyler. Derfor får du chokolademælk og ikke en lavalampe i et glas!
hver ublandbar væske kaldes en fase. En blanding med to ublandbare væsker kaldes en bifasisk blanding. En blanding med mere end to ublandbare væsker kaldes en flerfasisk blanding.
når du ser Globerne flyde rundt i en lavalampe, ser du på en bifasisk blanding!
vidste du det?
Globerne i en lavalampe er lavet af paraffinvoks. Det er den samme type voks, der bruges i mange stearinlys og farveblyanter!
hvorfor bevæger Globerne i en lavalampe sig rundt?
et af de mest interessante træk ved en lavalampe er den måde, hvorpå Globerne flyder rundt. Men hvorfor sker dette? Du ved, at Globerne er mindre tætte end den omgivende væske. Og du ved, at Globerne og væsken er ublandelige. Så hvorfor stiger Globerne ikke bare til toppen af lampen og bliver der?
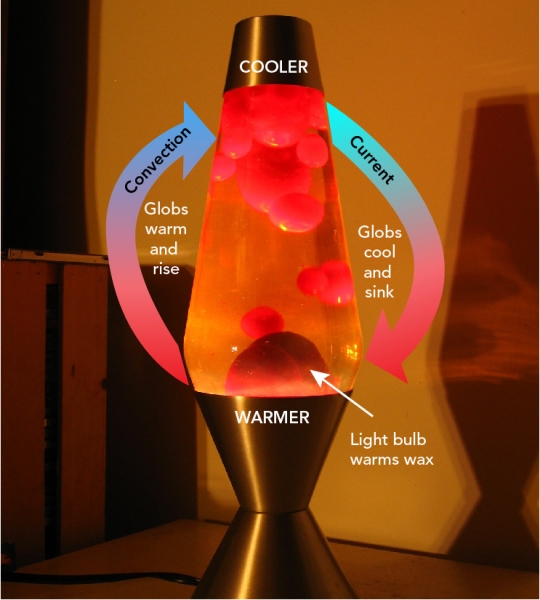
Nå, lavalamper er designet således, at temperaturen øverst er lidt køligere end i bunden. Og hvad sker der med molekyler, når de køler ned? Det er rigtigt! De mister energi og bevæger sig tættere sammen. Så når en glob når toppen af lavalampen, trækker den sig sammen. Det bliver tættere end den omgivende væske og begynder at synke. Når den når bunden, gentages hele cyklussen!
en lavalampe er et eksempel på en konvektionsstrøm. Konvektionsstrømme får væsker og gasser til at stige og falde på grund af ændringer i deres tæthed. Der er konvektionsstrømme rundt omkring dig, selv i jordskorpen!
vil du prøve et Lavalampeeksperiment?
Du kan bygge din egen lavalampe i dit klasseværelse eller derhjemme! Her er hvad du har brug for:
-
en gennemsigtig beholder, som en tom vand-eller sodavandflaske
-
vand
-
vegetabilsk olie
-
madfarvning
-
en brusetablet (som Alka-Seltser)
-
en lommelygte (som Alka-Seltser)
-
en lommelygte (som Alka-Seltser)
-
en valgfrit)
Sådan laver du en lavalampe:
-
Fyld en fjerdedel af flasken med vand
-
Tilføj madfarvning
-
fyld resten af flasken med vegetabilsk olie
-
Tilføj en halv brusetablet
-
valgfrit: hvis du har en lommelygte, skal du gå til et mørkt rum, tænde lommelygten og se din groovy nye lampe i mørket!
Leave a Reply