4.4: caracteristicile legăturilor covalente
electronegativitatea și polaritatea legăturii
deși am definit legătura covalentă ca partajare a electronilor, electronii dintr-o legătură covalentă nu sunt întotdeauna împărțiți în mod egal de cei doi atomi legați. Cu excepția cazului în care legătura conectează doi atomi ai aceluiași element, ca în H2, va exista întotdeauna un atom care atrage electronii în legătură mai puternic decât celălalt atom, ca în HCl, prezentat în figura \(\PageIndex{1}\). O legătură covalentă care are o împărțire egală a electronilor (figura \(\PageIndex{1a}\)) se numește o legătură covalentă nepolară. O legătură covalentă care are o împărțire inegală a electronilor, ca în figura \(\PageIndex{1b}\), se numește o legătură covalentă polară.

figura \(\PageIndex{1}\) legături covalente polare versus nepolare. (a) electronii din legătura covalentă sunt împărțiți în mod egal de ambii atomi de hidrogen. Aceasta este o legătură covalentă nepolară. (b) atomul de clor atrage electronii din legătură mai mult decât atomul de hidrogen, ducând la un dezechilibru în distribuția electronilor. Aceasta este o legătură covalentă polară.
distribuția densității electronilor într-o legătură polară este inegală. Este mai mare în jurul atomului care atrage electronii mai mult decât celălalt. De exemplu, electronii din legătura H–Cl a unei molecule de clorură de hidrogen petrec mai mult timp lângă atomul de clor decât lângă atomul de hidrogen. Rețineți că zona umbrită din jurul Cl din Figura \(\PageIndex{1b}\) este mult mai mare decât cea din jurul H.
acest dezechilibru al densității electronilor are ca rezultat o acumulare de sarcină negativă parțială (desemnată ca fiind−) pe o parte a legăturii (Cl) și o sarcină pozitivă parțială (desemnată ca -) pe cealaltă parte a legăturii (H). Acest lucru este văzut în figura \(\PageIndex{2a}\). Separarea sarcinii într-o legătură covalentă polară are ca rezultat un dipol electric (doi poli), reprezentat de săgeata din Figura \(\PageIndex{2b}\). Direcția săgeții este îndreptată spre capătul X-X, în timp ce coada+ a săgeții indică capătul X-X + al legăturii.
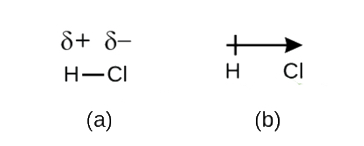
figura \(\PageIndex{2}\): (a) împărțirea inegală a perechii de electroni de legătură între H și Cl duce la sarcină pozitivă parțială pe atomul H și sarcină negativă parțială pe Cl. Simbolurile sec + și SEC-indică polaritatea legăturii H-Cl. (b) dipolul este reprezentat de o săgeată cu o cruce la coadă. Crucea se află în apropierea capătului sec.
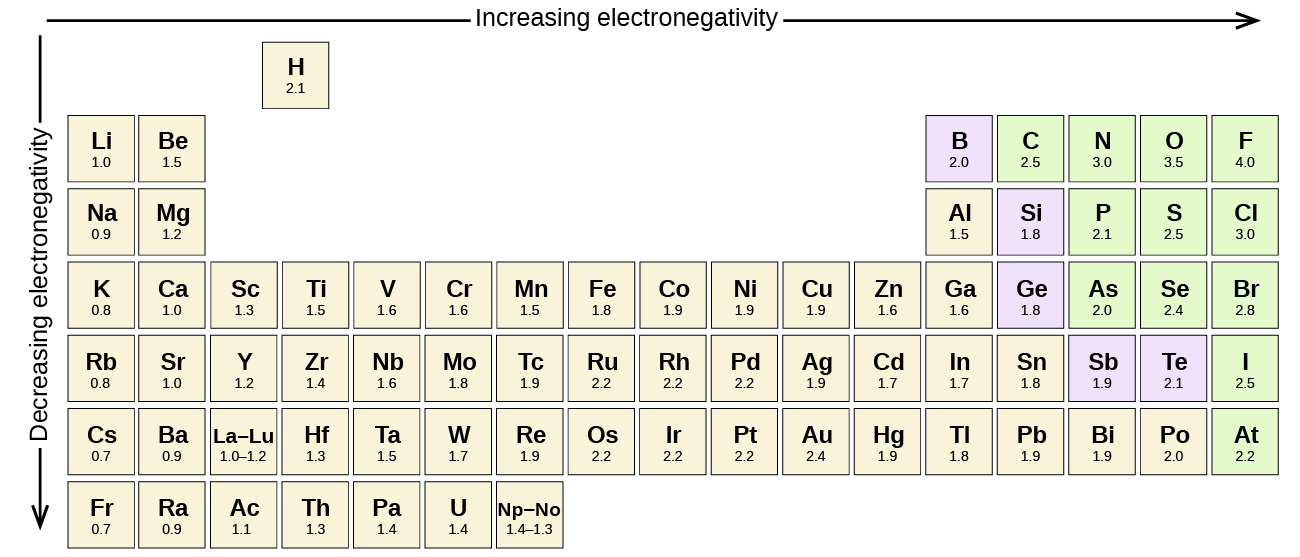
orice legătură covalentă între atomii diferitelor elemente este o legătură polară, dar gradul de polaritate variază foarte mult. Unele legături între diferite elemente sunt doar minim polare, în timp ce altele sunt puternic polare. Legăturile ionice pot fi considerate ultima în polaritate, electronii fiind transferați mai degrabă decât împărțiți. Pentru a judeca polaritatea relativă a unei legături covalente, chimiștii folosesc electronegativitate, care este o măsură relativă a cât de puternic atrage un atom electroni atunci când formează o legătură covalentă. Există diferite scale numerice pentru evaluarea electronegativității. Figura \(\PageIndex{3}\) prezintă una dintre cele mai populare—scara Pauling.
privind mai aproape: Fără îndoială, cel mai influent chimist al secolului 20, Linus Pauling (1901-94) este singura persoană care a câștigat două Premii Nobel individuale (adică nepartajate). În anii 1930, Pauling a folosit noi teorii matematice pentru a enunța unele principii fundamentale ale legăturii chimice. Cartea sa din 1939 natura legăturii chimice este una dintre cele mai semnificative cărți publicate vreodată în chimie.până în 1935, interesul lui Pauling s-a îndreptat către moleculele biologice și a primit Premiul Nobel pentru Chimie din 1954 pentru munca sa asupra structurii proteinelor. (El a fost foarte aproape de a descoperi structura dublu helix a ADN-ului când James Watson și James Crick au anunțat propria lor descoperire a structurii sale în 1953. Ulterior a primit Premiul Nobel pentru Pace din 1962 pentru eforturile sale de a interzice testarea armelor nucleare.

Linus Pauling a fost unul dintre cei mai influenți chimiști ai secolului 20.în ultimii săi ani, Pauling a devenit convins că dozele mari de vitamina C ar preveni bolile, inclusiv răceala obișnuită. Majoritatea cercetărilor clinice nu au reușit să arate o legătură, dar Pauling a continuat să ia doze mari zilnic. A murit în 1994, după ce a petrecut o viață întreagă stabilind o moștenire științifică pe care puțini o vor egala vreodată.
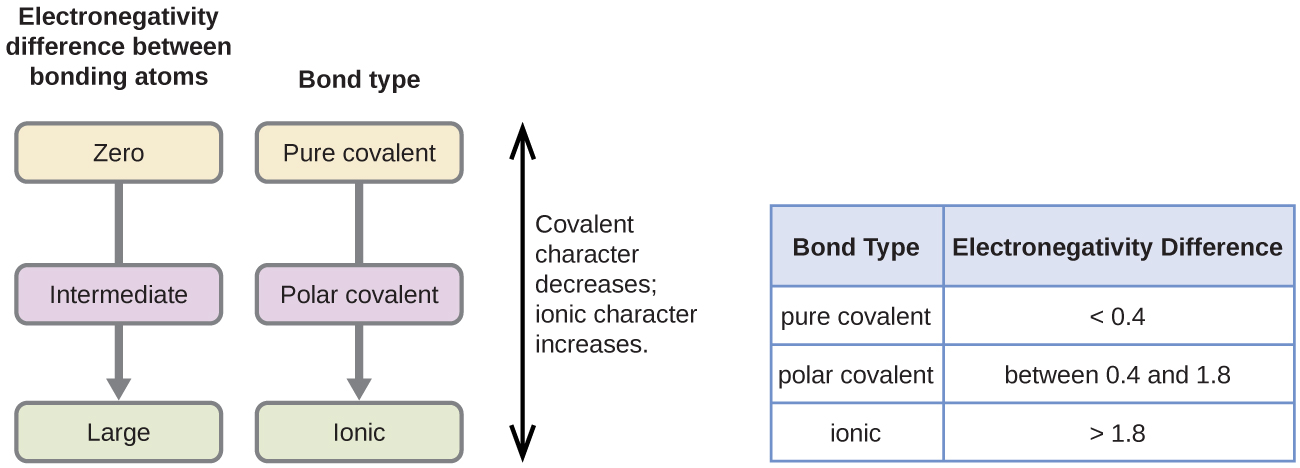
polaritatea unei legături covalente poate fi judecată prin determinarea diferenței de electronegativități a celor doi atomi care fac legătura. Cu cât este mai mare diferența de electronegativități, cu atât este mai mare dezechilibrul partajării electronilor în legătură. Deși nu există reguli dure și rapide, regula generală este dacă diferența de electronegativități este mai mică de aproximativ 0.4, legătura este considerată nepolară; dacă diferența este mai mare de 0,4, legătura este considerată polară. Dacă diferența de electronegativități este suficient de mare (în general mai mare de aproximativ 1,8), compusul rezultat este considerat ionic mai degrabă decât covalent. O diferență de electronegativitate de zero, desigur, indică o legătură covalentă nepolară.
Example \(\PageIndex{1}\)
descrieți diferența de electronegativitate dintre fiecare pereche de atomi și polaritatea rezultată (sau tipul de legătură).
- C și H
- H și H
- Na și Cl
- o și H
soluție
- carbonul are o electronegativitate de 2,5, în timp ce valoarea pentru hidrogen este de 2,1. Diferența este de 0,4, ceea ce este destul de mic. Prin urmare, legătura C–H este considerată nepolară.
- ambii atomi de hidrogen au aceeași valoare de electronegativitate—2.1. Diferența este zero, deci legătura este nepolară.electronegativitatea sodiului este de 0,9, în timp ce cea a clorului este de 3,0. Diferența este de 2,1, care este destul de mare, astfel încât sodiul și clorul formează un compus ionic.
- cu 2,1 pentru hidrogen și 3,5 pentru oxigen, diferența de electronegativitate este de 1,4. Ne-am aștepta la o legătură foarte polară. Împărțirea electronilor între o și H este inegală cu electronii mai puternic atrași spre O.
exercițiu \(\PageIndex{1}\)
descrieți diferența de electronegativitate (EN) dintre fiecare pereche de atomi și polaritatea rezultată (sau tipul de legătură).
- C și O
- K și Br
- N și n
- Cs și F
Răspuns a:
diferența EN este 1.0 , deci polar. Împărțirea electronilor între C și o este inegală cu electronii mai puternic atrași spre O.
răspuns b:
diferența EN este mai mare de 1,8, deci Ionică.
răspuns c:
atomii identici au zero en diferență, deci nepolar.
răspunsul d:
diferența EN este mai mare de 1,8, deci Ionică.
Leave a Reply