4.4: kovalenttisten sidosten ominaisuudet
elektronegatiivisuus ja sidoksen polariteetti
vaikka määrittelimme kovalenttisen sidoksen elektronien jakamiseksi, eivät kovalenttisen sidoksen elektronit aina jakaudu tasan kahden sidosatomin kesken. Ellei sidos yhdistä kahta saman alkuaineen atomia, kuten H2: ssa, on aina yksi atomi, joka vetää sidoksessa olevia elektroneja puoleensa voimakkaammin kuin toinen atomi, kuten HCl: ssä, joka on esitetty kuvassa \(\PageIndex{1}\). Kovalenttista sidosta, jolla on yhtä suuri osuus elektroneja (Kuva \(\PageIndex{1a}\)), kutsutaan ei-polaariseksi kovalenttiseksi sidokseksi. Kovalenttista sidosta, jolla on epätasaisesti jakautunut elektroneja, kuten kuvassa \(\PageIndex{1b}\), kutsutaan polaariseksi kovalenttiseksi sidokseksi.

kuva \(\PageIndex{1}\) polaarinen vs. ei-polaarinen kovalenttinen sidos. a) molemmat vetyatomit jakavat kovalenttisen sidoksen elektronit tasan. Tämä on ei-polaarinen kovalenttinen sidos. B) klooriatomi vetää sidoksessa olevia elektroneja puoleensa enemmän kuin vetyatomi, mikä johtaa elektronijakauman epätasapainoon. Tämä on napainen kovalenttinen sidos.
elektronitiheyden jakauma polaarisidoksessa on epätasainen. Se on suurempi atomin ympärillä, joka vetää elektroneja enemmän puoleensa kuin toinen. Esimerkiksi vetykloridimolekyylin h–cl-sidoksen elektronit viettävät enemmän aikaa klooriatomin kuin vetyatomin lähellä. Huomaa, että varjostettu alue Cl: n ympärillä Kuvassa \(\PageIndex{1b}\) on paljon suurempi kuin se on h: n ympärillä.
Tämä elektronitiheyden epätasapaino johtaa osittaisen negatiivisen varauksen (nimetty δ−) kertymiseen sidoksen toiselle puolelle (Cl) ja osittaisen positiivisen varauksen (nimetty δ+) kertymiseen sidoksen toiselle puolelle (H). Tämä näkyy kuvassa \(\PageIndex{2a}\). Varauksen erottaminen polaarisessa kovalenttisessa sidoksessa johtaa sähköiseen Dipoliin (kaksi napaa), jota kuvaa nuoli Kuvassa \(\PageIndex{2b}\). Nuolen suunta osoittaa kohti δ-päätä, kun taas nuolen pyrstö + osoittaa sidoksen δ+ – päätä.
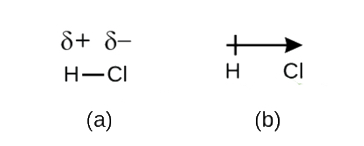
kuva \(\PageIndex{2}\): (a) sidoselektroniparin epätasainen jakautuminen H: n ja Cl: n välillä johtaa osittaiseen positiiviseen varaukseen h-atomissa ja osittaiseen negatiiviseen varaukseen Cl: ssä. Symbolit δ+ Ja δ-ilmaisevat h–Cl-sidoksen napaisuutta. b) Dipolia edustaa nuoli, jonka pyrstössä on risti. Risti on lähellä δ+–päätä ja nuolenpää yhtyy δ -.
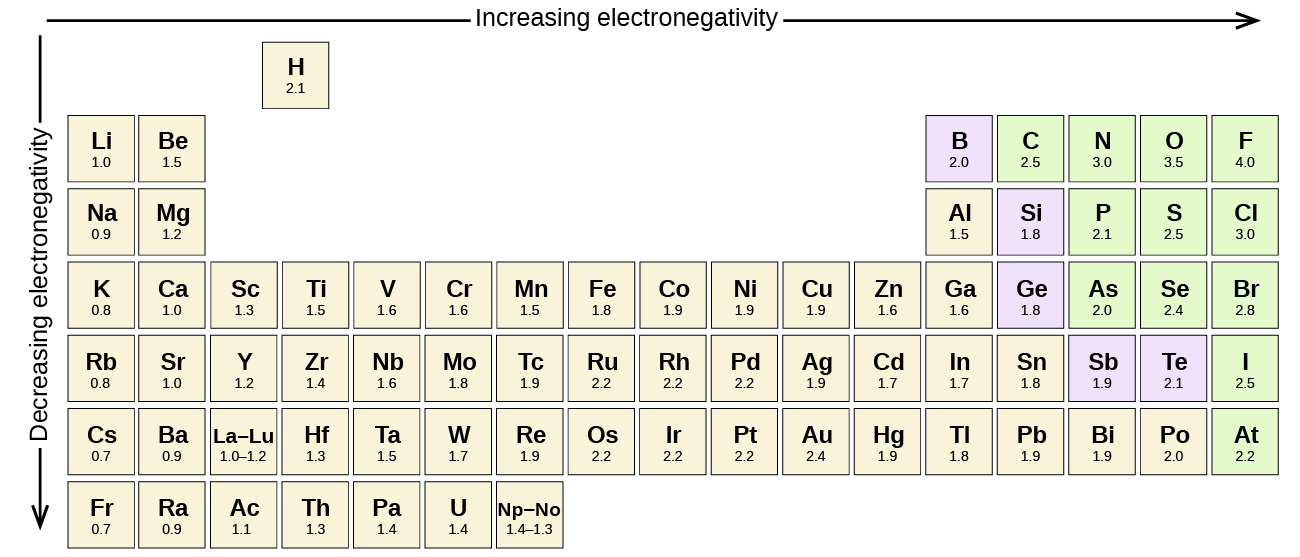
mikä tahansa kovalenttinen sidos eri alkuaineiden atomien välillä on polaarisidos, mutta polaarisuuden aste vaihtelee suuresti. Jotkut sidokset eri alkuaineiden välillä ovat vain minimaalisesti polaarisia, kun taas toiset ovat voimakkaasti polaarisia. Ionisidoksia voidaan pitää polariteetin perimmäisinä, jolloin elektroneja siirretään eikä jaeta. Kovalenttisen sidoksen suhteellisen napaisuuden arvioimiseksi kemistit käyttävät elektronegatiivisuutta, joka on suhteellinen mitta sille, kuinka voimakkaasti atomi vetää elektroneja puoleensa muodostaessaan kovalenttisen sidoksen. On olemassa erilaisia numeerisia asteikkoja luokitus elektronegatiivisuus. Kuvassa \(\PageIndex{3}\) näkyy yksi suosituimmista—Pauling-asteikko.
Looking Closer: Linus Pauling
kiistatta 1900-luvun vaikutusvaltaisin kemisti Linus Pauling (1901-94) on ainoa henkilö, joka on voittanut kaksi yksittäistä (eli korutonta) Nobelia. 1930-luvulla Pauling käytti uusia matemaattisia teorioita esittääkseen joitakin kemiallisen sidoksen perusperiaatteita. Hänen vuonna 1939 ilmestynyt kirjansa ”The Nature of the Chemical Bond” on yksi merkittävimmistä kemian alalta koskaan julkaistuista kirjoista.
vuoteen 1935 mennessä Paulingin kiinnostus kääntyi biologisiin molekyyleihin, ja hän sai 1954 Nobelin kemianpalkinnon työstään proteiinin rakenteen parissa. (Hän oli hyvin lähellä DNA: n kaksoiskierteen rakenteen löytämistä, kun James Watson ja James Crick ilmoittivat omasta löydöstään sen rakenteesta vuonna 1953.) Hänelle myönnettiin myöhemmin vuoden 1962 Nobelin rauhanpalkinto pyrkimyksistään kieltää ydinaseiden testaus.

Linus Pauling oli 1900-luvun vaikutusvaltaisimpia kemistejä.
myöhempinä vuosinaan Pauling vakuuttui siitä, että suuret C-vitamiiniannokset ehkäisisivät sairauksia, muun muassa flunssaa. Useimmat kliiniset tutkimukset eivät osoittaneet yhteyttä, mutta Pauling jatkoi suurten annosten ottamista päivittäin. Hän kuoli vuonna 1994, vietettyään eliniän luomalla tieteellisen perinnön, jota harvat tulevat koskaan vertaamaan.
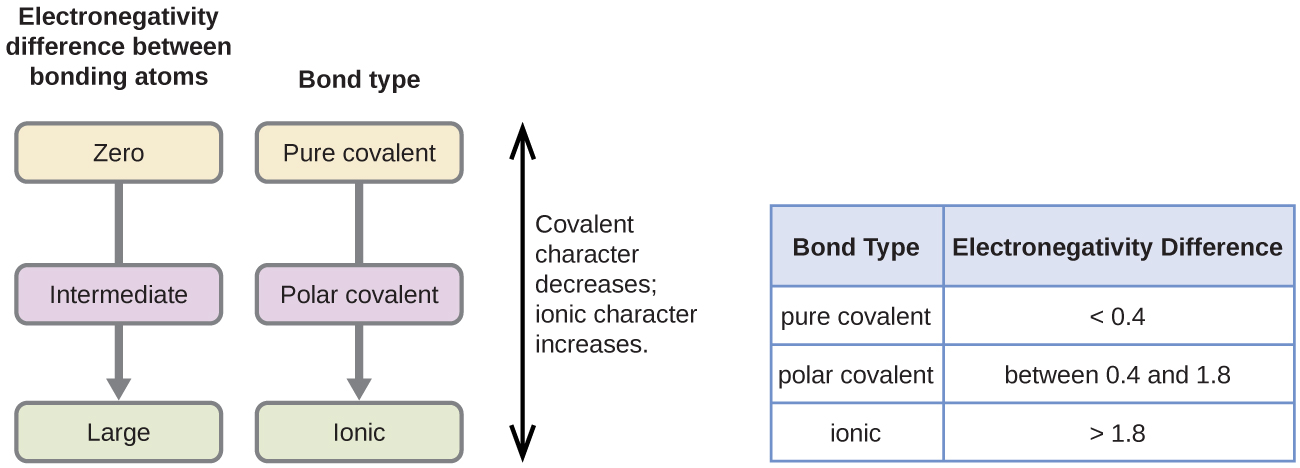
kovalenttisen sidoksen polaarisuus voidaan arvioida määrittämällä sidoksen muodostavien kahden atomin elektronegatiivisuuksien ero. Mitä suurempi ero elektronegatiivisuuksissa on, sitä suurempi on elektronin jakautumisen epätasapaino sidoksessa. Vaikka kovia ja nopeita sääntöjä ei ole, yleissääntö on, jos elektronegatiivisuuksien ero on alle 0.4, sidosta pidetään ei-polaarisena; jos ero on suurempi kuin 0,4, sidosta pidetään polaarisena. Jos ero elektronegatiivisuuksissa on riittävän suuri (yleensä suurempi kuin noin 1,8), muodostuvaa yhdistettä pidetään ennemmin ionisena kuin kovalenttisena. Elektronegatiivisuusero nolla, tietenkin, osoittaa ei-polaarinen kovalenttinen sidos.
esimerkki \(\PageIndex{1}\)
kuvaa kunkin atomiparin elektronegatiivisuuseroa ja siitä johtuvaa napaisuutta (tai sidostyyppiä).
- C ja H
- H ja h
- Na ja Cl
- O ja h
liuos
- hiilen elektronegatiivisuus on 2,5, kun taas vedyn arvo on 2,1. Ero on 0,4, mikä on melko pieni. C-H-joukkovelkakirjalainaa pidetään sen vuoksi ei-polaarisena.
- molemmilla vetyatomeilla on sama elektronegatiivisuusarvo—2,1. Ero on nolla, joten sidos on nonpolaarinen.
- natriumin elektronegatiivisuus on 0,9, kun taas kloorin on 3,0. Ero on 2,1 eli melko suuri, joten natrium ja kloori muodostavat ioniyhdisteen.
- kun vedyllä on 2,1 ja hapella 3,5, elektronegatiivisuusero on 1,4. Odottaisimme hyvin polaarista sidettä. Elektronien jakaantuminen O: n ja H: n välillä on epätasa-arvoista O: ta kohti voimakkaammin vedettyjen elektronien kanssa.
Exercise \(\PageIndex{1}\)
Describe the electronegativity (En) difference between each par of atoms and the resulting polarity (or bond type).
- C ja o
- N ja n
- cs ja F
ja Br
vastaus A:
EN-ero on 1,0 eli polaarinen. Elektronien jakaantuminen C: n ja O: n välillä on epätasa-arvoista O: n suuntaan voimakkaammin piirrettyjen elektronien kanssa.
vastaus b:
EN-ero on suurempi kuin 1,8, eli ioninen.
Vastaus c:
identtisillä atomeilla on nolla EN-ero, eli nonpolaarinen.
vastaus d:
EN-ero on suurempi kuin 1,8, eli ioninen.
Leave a Reply