4.4: Caratteristiche dei legami covalenti
Elettronegatività e polarità del legame
Sebbene abbiamo definito il legame covalente come condivisione di elettroni, gli elettroni in un legame covalente non sono sempre condivisi equamente dai due atomi legati. A meno che il legame non colleghi due atomi dello stesso elemento, come in H2, ci sarà sempre un atomo che attrae gli elettroni nel legame più fortemente dell’altro atomo, come in HCl, mostrato in Figura \(\PageIndex{1}\). Un legame covalente che ha una condivisione uguale di elettroni (Figura \ (\PageIndex{1a}\)) è chiamato legame covalente non polare. Un legame covalente che ha una condivisione disuguale di elettroni, come in Figura \(\PageIndex{1b}\), è chiamato un legame covalente polare.

Figura \(\PageIndex{1}\) Legami covalenti polari rispetto a legami covalenti non polari. (a) Gli elettroni nel legame covalente sono equamente condivisi da entrambi gli atomi di idrogeno. Questo è un legame covalente non polare. (b) L’atomo di cloro attira gli elettroni nel legame più dell’atomo di idrogeno, portando ad uno squilibrio nella distribuzione degli elettroni. Questo è un legame covalente polare.
La distribuzione della densità elettronica in un legame polare non è uniforme. È maggiore intorno all’atomo che attrae gli elettroni più dell’altro. Ad esempio, gli elettroni nel legame H–Cl di una molecola di cloruro di idrogeno trascorrono più tempo vicino all’atomo di cloro che vicino all’atomo di idrogeno. Si noti che l’area ombreggiata attorno a Cl nella figura \(\PageIndex{1b}\) è molto più grande di quella attorno a H.
Questo squilibrio nella densità elettronica provoca un accumulo di carica negativa parziale (designata come δ−) su un lato del legame (Cl) e una carica positiva parziale (designata δ+) sull’altro lato del legame (H). Questo è visto in Figura \(\PageIndex{2a}\). La separazione della carica in un legame covalente polare si traduce in un dipolo elettrico (due poli), rappresentato dalla freccia in figura \(\PageIndex{2b}\). La direzione della freccia è rivolta verso l’estremità δ mentre la coda + della freccia indica l’estremità δ+ del legame.
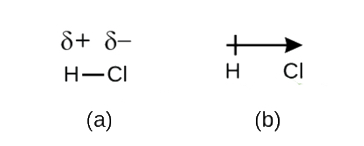
Figura \(\PageIndex{2}\): (a) La condivisione disuguale della coppia di elettroni di legame tra H e Cl porta alla carica positiva parziale sull’atomo H e alla carica negativa parziale sul Cl. I simboli δ + e δ-indicano la polarità del legame H–Cl. (b) Il dipolo è rappresentato da una freccia con una croce alla coda. La croce è vicino alla fine δ + e la punta della freccia coincide con il δ -.
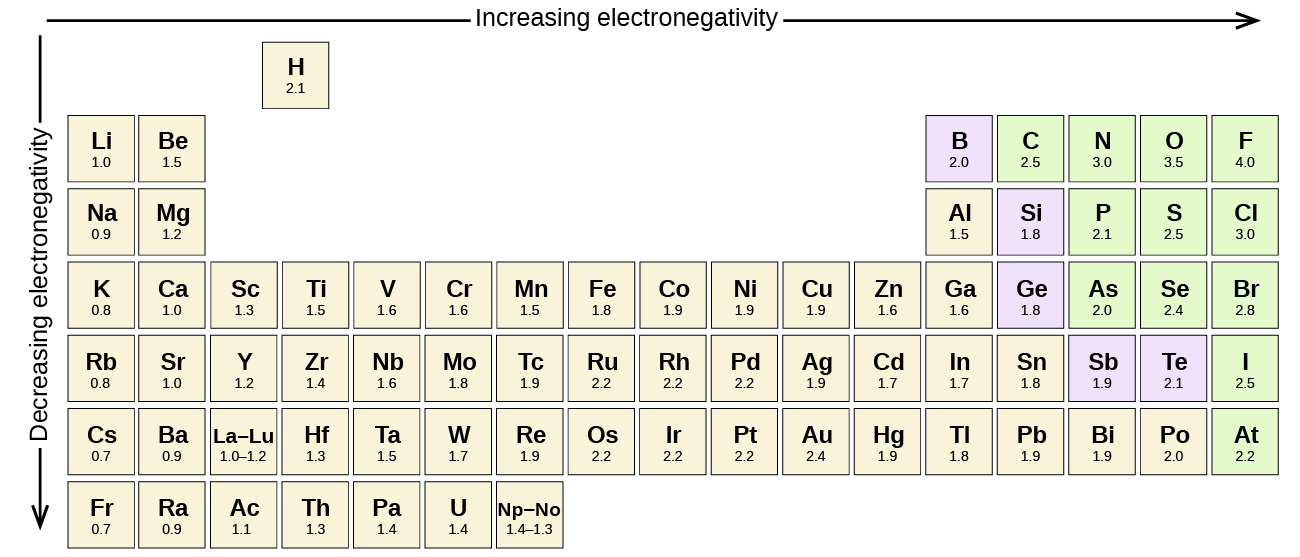
Qualsiasi legame covalente tra atomi di elementi diversi è un legame polare, ma il grado di polarità varia ampiamente. Alcuni legami tra diversi elementi sono solo minimamente polari, mentre altri sono fortemente polari. I legami ionici possono essere considerati l’ultimo in polarità, con elettroni trasferiti piuttosto che condivisi. Per giudicare la polarità relativa di un legame covalente, i chimici usano l’elettronegatività, che è una misura relativa di quanto fortemente un atomo attrae gli elettroni quando forma un legame covalente. Esistono varie scale numeriche per valutare l’elettronegatività. Figura \(\PageIndex{3}\) mostra uno dei più popolari—la scala Pauling.
Guardando più da vicino: Linus Pauling
Probabilmente il chimico più influente del 20 ° secolo, Linus Pauling (1901-94) è l’unica persona ad aver vinto due premi Nobel individuali (cioè non condivisi). Nel 1930, Pauling utilizzato nuove teorie matematiche per enunciare alcuni principi fondamentali del legame chimico. Il suo libro del 1939 The Nature of the Chemical Bond è uno dei libri più significativi mai pubblicati in chimica.
Nel 1935, l’interesse di Pauling si rivolse alle molecole biologiche e nel 1954 ricevette il Premio Nobel per la chimica per il suo lavoro sulla struttura delle proteine. (Era molto vicino a scoprire la struttura a doppia elica del DNA quando James Watson e James Crick annunciarono la loro scoperta della sua struttura nel 1953. In seguito fu insignito del Premio Nobel per la Pace nel 1962 per i suoi sforzi volti a vietare i test di armi nucleari.

Linus Pauling è stato uno dei chimici più influenti del xx secolo.
Nei suoi ultimi anni, Pauling si convinse che grandi dosi di vitamina C avrebbero prevenuto le malattie, incluso il comune raffreddore. La maggior parte delle ricerche cliniche non è riuscita a mostrare una connessione, ma Pauling ha continuato a prendere grandi dosi al giorno. Morì nel 1994, dopo aver trascorso una vita a stabilire un’eredità scientifica che pochi potranno mai eguagliare.
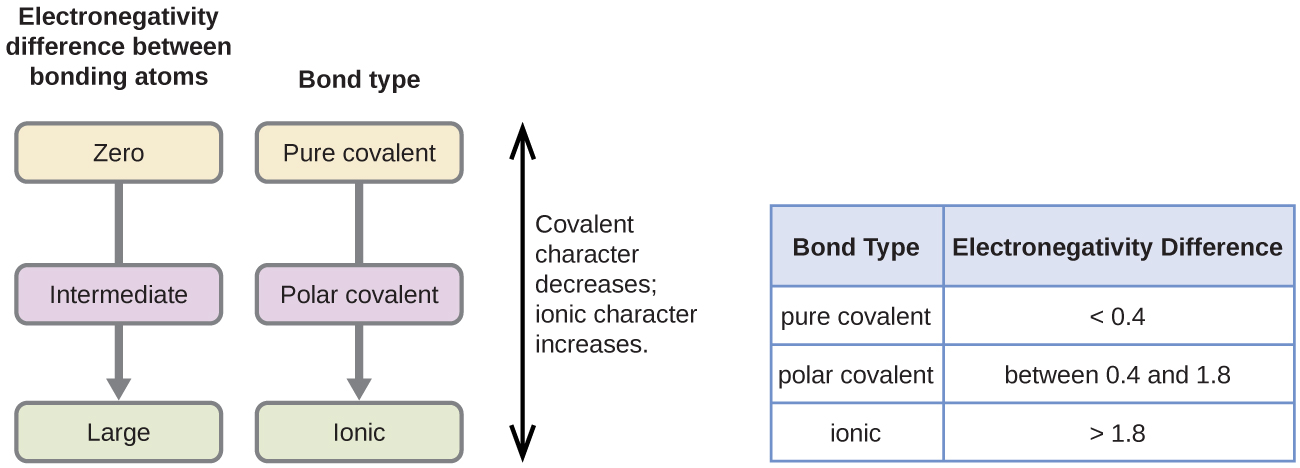
La polarità di un legame covalente può essere giudicata determinando la differenza nelle elettronegatività dei due atomi che formano il legame. Maggiore è la differenza di elettronegatività, maggiore è lo squilibrio della condivisione degli elettroni nel legame. Anche se non ci sono regole dure e veloci, la regola generale è se la differenza di elettronegatività è inferiore a circa 0.4, il legame è considerato non polare; se la differenza è maggiore di 0,4, il legame è considerato polare. Se la differenza di elettronegatività è abbastanza grande (generalmente maggiore di circa 1,8), il composto risultante è considerato ionico piuttosto che covalente. Una differenza di elettronegatività pari a zero, ovviamente, indica un legame covalente non polare.
Esempio \(\PageIndex{1}\)
Descrivere la differenza di elettronegatività tra ogni coppia di atomi e la polarità risultante (o tipo di legame).
- C e H
- H e H
- Na e Cl
- O e H
Soluzione
- il Carbonio ha una elettronegatività di 2,5, mentre il valore di idrogeno è di 2.1. La differenza è 0,4, che è piuttosto piccola. Il legame C-H è quindi considerato non polare.
- Entrambi gli atomi di idrogeno hanno lo stesso valore di elettronegatività-2.1. La differenza è zero, quindi il legame è non polare.
- L’elettronegatività del sodio è 0,9, mentre quella del cloro è 3,0. La differenza è 2.1, che è piuttosto alta, e quindi sodio e cloro formano un composto ionico.
- Con 2.1 per l’idrogeno e 3.5 per l’ossigeno, la differenza di elettronegatività è 1.4. Ci aspetteremmo un legame molto polare. La condivisione di elettroni tra O e H è disuguale con gli elettroni più fortemente attratti verso O.
Esercizio \(\PageIndex{1}\)
Descrivere la differenza di elettronegatività (EN) tra ogni coppia di atomi e la polarità risultante (o tipo di legame).
- C e O
- K e Br
- N e N
- Cs e F
Risposta a:
La differenza EN è 1.0 , quindi polare. La condivisione di elettroni tra C e O è disuguale con gli elettroni più fortemente attratti verso O.
Risposta b:
La differenza EN è maggiore di 1,8, quindi ionica.
Risposta c:
Gli atomi identici hanno zero EN differenza, quindi non polare.
Risposta d:
La differenza EN è maggiore di 1,8, quindi ionica.
Leave a Reply