15.3: fysiske egenskaber af Carboksyl syrer
læringsmål
- Sammenlign kogepunkterne for carboksyl syrer med alkoholer med lignende molmasse.
- Sammenlign opløselighederne af carboksyl syrer i vand med opløselighederne af sammenlignelige alkaner og alkoholer i vand.
mange carboksyl syrer er farveløse væsker med ubehagelige lugte. 5 til 10 carbonatomer har alle” goaty ” lugt (forklarer lugten af Limburger ost). Disse syrer produceres også ved virkningen af hudbakterier på humant talg (hudolier), der tegner sig for lugten af dårligt ventilerede skabsrum. Syrerne med mere end 10 carbonatomer er vokslignende faste stoffer, og deres lugt mindskes med stigende molær masse og resulterende faldende volatilitet.
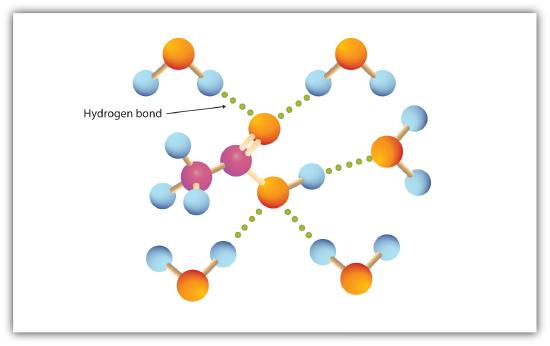
carboksyliske syrer udviser stærk hydrogenbinding mellem molekyler. De har derfor høje kogepunkter sammenlignet med andre stoffer med sammenlignelig molmasse.gruppen engagerer sig let i hydrogenbinding med vandmolekyler (figur \(\Sideindeks{1}\)). Syrerne med et til fire carbonatomer er fuldstændigt blandbare med vand. Opløseligheden falder, når carbonkædelængden øges, fordi dipolkræfter bliver mindre vigtige, og dispersionskræfter bliver mere dominerende. 1,0 g / 100 g vand). Palmitinsyre med sin store ikke-polære carbonhydridkomponent er i det væsentlige uopløselig i vand. De er generelt opløselige i sådanne organiske opløsningsmidler som ethanol, toluen og diethylether.
tabel 15.4.1 viser nogle fysiske egenskaber for udvalgte carboksyl syrer. De første seks er homologer. Bemærk, at kogepunkterne stiger med stigende molmasse, men smeltepunkterne viser intet regelmæssigt mønster.
| Condensed Structural Formula | Name of Acid | Melting Point (°C) | Boiling Point (°C) | Solubility (g/100 g of Water) |
|---|---|---|---|---|
| HCOOH | formic acid | 8 | 100 | miscible |
| CH3COOH | acetic acid | 17 | 118 | miscible |
| CH3CH2COOH | propionic acid | –22 | 141 | miscible |
| CH3(CH2)2COOH | butyric acid | –5 | 163 | miscible |
| CH3(CH2)3COOH | valeric acid | –35 | 187 | 5 |
| CH3(CH2)4COOH | caproic acid | –3 | 205 | 1.1 |
| C6H5COOH | benzoic acid | 122 | 249 | 0.29 |
Concept Review Exercises
- Which compound has the higher boiling point—butanoic acid (molar mass 88) or 2-pentanone (molar mass 86)? Explain.
- Would you expect butyric acid (butanoic acid) to be more or less soluble than 1-butanol in water? Explain.
svar
- smørsyre på grund af hydrogenbinding (der er ingen intermolekylær hydrogenbinding i 2-pentanon.)
- mere opløselig, fordi der er mere omfattende hydrogenbinding
nøgle grillbarer
- Carboksyl syrer har høje kogepunkter sammenlignet med andre stoffer med sammenlignelig molær masse. Kogepunkter øges med molær masse.
- carboksyl syrer med et til fire carbonatomer er fuldstændig blandbare med vand. Opløseligheden falder med molær masse.
øvelser
-
hvilken forbindelse har det højere kogepunkt-CH3CH2CH2OCH2CH3 eller CH3CH2CH2COOH? Forklare.
-
hvilken forbindelse har det højere kogepunkt-CH3CH2CH2CH2CH2OH eller CH3CH2CH2COOH? Forklare.
-
hvilken forbindelse er mere opløselig i vand—CH3COOH eller CH3CH2CH2CH3? Forklare.
-
hvilken forbindelse er mere opløselig i vand—CH3CH2COOH eller CH3CH2CH2CH2CH2COOH? Forklare.
svar
-
CH3CH2CH2COOH på grund af hydrogenbinding (der er ingen intermolekylær hydrogenbinding med CH3CH2CH2OCH2CH3.)
-
CH3COOH fordi det engagerer sig i hydrogenbinding med vand (der er ingen intermolekylær hydrogenbinding med CH3CH2CH2CH3.)
Leave a Reply