Cetirizine
Generic Name: Cetirizine hydrochloride
Dosage Form: oral solution
Medically reviewed by Drugs.com. Last updated on Feb 1, 2021.
- Overview
- Side Effects
- Dosage
- Professional
- Tips
- Interactions
- More
Cetirizine HYDROCHLORIDE ORAL SOLUTION, USP
For Oral Use
Rx Only
Cetirizine Description
Cetirizine hydrochloride is an orally active and selective H1-receptor antagonist. Denumirea chimică este de (±) – -1 – piperazinyl] etoxi] acid acetic, diclorhidrat. Clorhidratul de cetirizină este un compus racemic cu o formulă empirică de C21H25ClN2O3 •2HCl. Greutatea moleculară este de 461,82, iar structura chimică este prezentată mai jos:
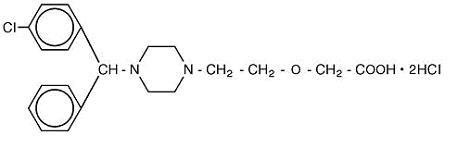
diclorhidratul de cetirizină este o pulbere albă sau aproape albă și este liber solubil în apă, practic insolubil în acetonă și în clorură de metilen. Soluție orală de clorhidrat de cetirizină, USP este o soluție orală incoloră până la ușor galbenă care conține clorhidrat de cetirizină la o concentrație de 1 mg/mL (5 mg/5 mL) pentru administrare orală. PH-ul este între 4 și 5. Ingredientele inactive ale soluției orale sunt: acid acetic glacial, aromă de struguri, glicerină, metilparaben, propilen glicol, propilparaben, acetat de sodiu, zaharoză și apă purificată.
Cetirizina-Farmacologie Clinică
mecanismul de acțiune: Cetirizina, un metabolit uman al hidroxizinei, este un antihistaminic; efectele sale principale sunt mediate prin inhibarea selectivă a receptorilor H1 periferici. Activitatea antihistaminică a cetirizinei a fost clar documentată într-o varietate de modele animale și umane. Modelele animale in vivo și ex vivo au prezentat activitate anticolinergică și anti-serotoninergică neglijabilă. Cu toate acestea, în studiile clinice, gura uscată a fost mai frecventă cu Cetirizina decât cu placebo. Studiile in vitro privind legarea receptorilor nu au arătat afinitate măsurabilă pentru alți receptori decât H1. Studiile autoradiografice cu cetirizină marcată radioactiv la șobolan au arătat o penetrare neglijabilă în creier. Experimentele Ex vivo la șoarece au arătat că cetirizina administrată sistemic nu ocupă în mod semnificativ receptorii H1 cerebrali.
farmacocinetica:
absorbție: Cetirizina a fost absorbită rapid cu un timp până la concentrația maximă (T max) de aproximativ 1 oră după administrarea orală de comprimate sau soluție orală la adulți. S-a constatat o biodisponibilitate comparabilă între forma de dozare a comprimatului și a soluției orale. Când voluntarilor sănătoși li s-au administrat doze multiple de cetirizină (comprimate de 10 mg o dată pe zi timp de 10 zile), s-a observat o concentrație plasmatică maximă medie (Cmax) de 311 ng/mL. Nu a fost observată acumularea. Farmacocinetica cetirizinei a fost liniară pentru dozele orale cuprinse între 5 și 60 mg. Alimentele nu au avut niciun efect asupra gradului de expunere la cetirizină (ASC), dar T max a fost întârziat cu 1, 7 ore, iar C max a scăzut cu 23% în prezența alimentelor.
distribuție: Legarea medie de proteinele plasmatice a cetirizinei este de 93%, independent de concentrația în intervalul 25-1000 ng/mL, care include concentrațiile plasmatice terapeutice observate.Metabolism: un studiu de echilibru al masei la 6 voluntari sănătoși de sex masculin a indicat că 70% din radioactivitatea administrată a fost recuperată în urină și 10% în fecale. Aproximativ 50% din radioactivitate a fost identificată în urină ca medicament nemodificat. Cea mai mare parte a creșterii rapide a radioactivității plasmatice maxime a fost asociată cu medicamentul părinte, sugerând un grad scăzut de metabolizare la primul pasaj hepatic. Cetirizina este metabolizată într-o măsură limitată prin o-dezalchilare oxidativă la un metabolit cu activitate antihistaminică neglijabilă. Enzima sau enzimele responsabile de acest metabolism nu au fost identificate.eliminare: timpul mediu de înjumătățire plasmatică prin eliminare la 146 de voluntari sănătoși în cadrul mai multor studii farmacocinetice a fost de 8,3 ore, iar clearance-ul aparent total al cetirizinei a fost de aproximativ 53 mL/min.
studii de interacțiune
studiile de interacțiune farmacocinetică cu cetirizină la adulți au fost efectuate cu pseudoefedrină, antipirină, ketoconazol, eritromicină și azitromicină.
nu s-au observat interacțiuni. Într-un studiu cu doze multiple de teofilină (400 mg o dată pe zi timp de 3 zile) și cetirizină (20 mg o dată pe zi timp de 3 zile), s-a observat o scădere cu 16% a clearance-ului cetirizinei. Distribuția teofilinei nu a fost modificată prin administrarea concomitentă de cetirizină.
populații speciale
Copii și adolescenți: La pacienții pediatri cu vârsta cuprinsă între 2 și 5 ani care au primit 5 mg de cetirizină, Media C max a fost de 660 ng/mL. Pe baza comparațiilor de studii încrucișate, greutatea normalizată, clearance-ul aparent total al corpului a fost cu 81-111% mai mare, iar timpul de înjumătățire plasmatică prin eliminare a fost cu 33 până la 41% mai scurt la populația pediatrică decât la adulți. La copii și adolescenți cu vârsta cuprinsă între 6 și 23 de luni care au primit o doză unică de 0,25 mg/kg soluție orală de cetirizină (doza medie de 2,3 mg), media Cmax a fost de 390 ng/mL. Pe baza comparațiilor între studii, clearance-ul total aparent normalizat în greutate a fost cu 304% mai mare, iar timpul de înjumătățire plasmatică prin eliminare a fost cu 63% mai scurt la această populație pediatrică comparativ cu adulții. ASC medie (0-t) la copii cu vârsta cuprinsă între 6 luni și < 2 ani care primesc doza maximă de soluție de cetirizină (2,5 mg de două ori pe zi) este de așteptat să fie de două ori mai mare decât cea observată la adulții care primesc o doză de 10 mg comprimate de cetirizină o dată pe zi.
efectul sexului: efectul sexului asupra farmacocineticii cetirizinei nu a fost studiat în mod adecvat.
efectul rasei: nu s-au observat diferențe legate de rasă în cinetica cetirizinei.
farmacodinamică: clorhidratul de cetirizină la doze de 5 și 10 mg a inhibat puternic wheal și flare cauzate de injectarea intradermică a histaminei la 19 voluntari pediatrici (cu vârsta cuprinsă între 5 și 12 ani) și activitatea a persistat timp de cel puțin 24 de ore. Într-un studiu de 35 de zile la copii cu vârsta cuprinsă între 5 și 12 ani, nu a fost găsită nicio toleranță la efectele antihistaminice (suprimarea răspunsului wheal și flare) ale clorhidratului de cetirizină. La 10 sugari cu vârsta cuprinsă între 7 și 25 de luni, cărora li s-a administrat cetirizină într-o soluție orală de 4 până la 9 zile (0, 25 mg/kg de două ori pe zi), s-a observat o inhibare de 90% a wheal cutanat indus de histamină (10 mg/mL) și o inhibare de 87% a flare la 12 ore după administrarea ultimei doze. Nu se cunoaște relevanța clinică a acestei suprimări a răspunsului indus de histamină la testele cutanate.efectele injectării intradermice a diferiților alți mediatori sau eliberatori de histamină au fost, de asemenea, inhibate de cetirizină, așa cum a fost răspunsul la o provocare la rece la pacienții cu urticarie indusă de frig. La subiecții ușor astmatici, clorhidratul de cetirizină la 5 până la 20 mg a blocat bronhoconstricția datorită histaminei nebulizate, cu blocaj practic total după o doză de 20 mg. În studiile efectuate timp de până la 12 ore după provocarea cutanată a antigenului, recrutarea în fază târzie a eozinofilelor, neutrofilelor și bazofilelor, componente ale răspunsului inflamator alergic, a fost inhibată de clorhidratul de cetirizină la o doză de 20 mg. În patru studii clinice la bărbați adulți sănătoși, nu s-au observat creșteri medii semnificative clinic ale QTc la subiecții tratați cu clorhidrat de cetirizină. În primul studiu, un studiu încrucișat controlat cu placebo, clorhidratul de cetirizină a fost administrat în doze de până la 60 mg pe zi, de 6 ori doza clinică maximă, timp de 1 săptămână și nu a apărut o prelungire medie semnificativă a QTc. În cel de-al doilea studiu, un studiu încrucișat, clorhidratul de cetirizină 20 mg și eritromicina (500 mg la fiecare 8 ore) au fost administrate singure și în asociere. Nu a existat niciun efect semnificativ asupra QTc cu asocierea sau numai cu clorhidrat de cetirizină. În cel de-al treilea studiu, de asemenea, un studiu încrucișat, clorhidratul de cetirizină 20 mg și ketoconazolul (400 mg pe zi) au fost administrate singure și în asociere.clorhidratul de cetirizină a determinat o creștere medie a QTc de 9,1 msec față de valoarea inițială după 10 zile de tratament. De asemenea, ketoconazolul a crescut QTc cu 8,3 msec. Combinația a provocat o creștere de 17,4 msec, egală cu suma efectelor individuale. Astfel, nu a existat o interacțiune semnificativă a medicamentului pe QTc cu combinația de clorhidrat de cetirizină și ketoconazol. În cel de-al patrulea studiu, un studiu paralel controlat cu placebo, clorhidratul de cetirizină 20 mg a fost administrat singur sau în asociere cu azitromicina (500 mg ca doză unică în prima zi urmată de 250 mg o dată pe zi). Nu a existat o creștere semnificativă a QTc cu clorhidrat de cetirizină 20 mg în monoterapie sau în asociere cu azitromicină. Într-un studiu clinic de patru săptămâni la copii și adolescenți cu vârsta cuprinsă între 6 și 11 ani, rezultatele măsurătorilor ECG obținute aleatoriu înainte de tratament și după 2 săptămâni de tratament au arătat că clorhidratul de cetirizină 5 sau 10 mg nu a crescut QTc comparativ cu placebo. Într-un studiu clinic de o săptămână (N=86) cu soluție orală de clorhidrat de cetirizină, USP (0, 25 mg/kg de două ori pe zi) comparativ cu placebo la copii și adolescenți cu vârsta cuprinsă între 6 și 11 luni, măsurătorile ECG efectuate în decurs de 3 ore de la ultima doză nu au evidențiat anomalii ECG sau creșteri ale intervalului QTc în niciunul dintre grupuri, comparativ cu evaluările inițiale. Datele din alte studii în care clorhidratul de cetirizină a fost administrat pacienților cu vârsta cuprinsă între 6-23 luni au fost în concordanță cu constatările din acest studiu.efectele clorhidratului de cetirizină asupra intervalului QTc la doze mai mari de 10 mg nu au fost studiate la copii cu vârsta mai mică de 12 ani. Într-un studiu de șase săptămâni, controlat cu placebo, la 186 de pacienți (cu vârsta cuprinsă între 12 și 64 de ani) cu rinită alergică și astm bronșic ușor până la moderat, clorhidratul de cetirizină 10 mg o dată pe zi a îmbunătățit simptomele rinitei și nu a modificat funcția pulmonară. Într-un studiu clinic de două săptămâni, controlat cu placebo, o analiză subset a 65 de pacienți cu rinită alergică pediatrică (cu vârsta cuprinsă între 6 și 11 ani) cu astm a arătat că clorhidratul de cetirizină nu modifică funcția pulmonară. Aceste studii susțin siguranța administrării clorhidratului de cetirizină la pacienții cu rinită alergică pediatrică și adultă cu astm ușor până la moderat.
studii clinice: studii clinice multicentrice, randomizate, dublu-orb, care au comparat Cetirizina 5 până la 20 mg cu placebo la pacienții cu vârsta de 12 ani și peste cu rinită alergică perenă au fost efectuate în Statele Unite. Două dintre acestea au prezentat reduceri semnificative ale simptomelor rinitei alergice perene timp de până la 8 săptămâni. De asemenea, au fost efectuate două studii clinice multicentrice, randomizate, dublu-orb, de 4 săptămâni, care au comparat Cetirizina 5 până la 20 mg cu placebo la pacienții cu urticarie idiopatică cronică și au arătat o îmbunătățire semnificativă a simptomelor urticariei idiopatice cronice. În general, doza de 10 mg a fost mai eficace decât doza de 5 mg, iar doza de 20 mg nu a dat niciun efect suplimentar. Unele dintre aceste studii au inclus pacienți pediatrici cu vârsta cuprinsă între 12 și 16 ani. În plus, patru studii multicentrice, randomizate, controlate cu placebo, dublu-orb de 2-4 săptămâni la 534 de pacienți pediatrici cu vârsta cuprinsă între 6 și 11 ani cu rinită alergică sezonieră au fost efectuate în Statele Unite la doze de până la 10 mg.
indicații& utilizare
rinită alergică perenă: soluție orală de clorhidrat de cetirizină, USP este indicat pentru ameliorarea simptomelor asociate cu rinita alergică perenă datorată alergenilor, cum ar fi acarienii de praf, părul animalelor și mucegaiurile la copii cu vârsta cuprinsă între 6 și 23 de luni. Simptomele tratate eficient includ strănutul, rinoreea, secreția postnasală, pruritul nazal, pruritul ocular și ruperea.
urticarie cronică: soluție orală de clorhidrat de cetirizină, USP este indicat pentru tratamentul manifestărilor cutanate necomplicate ale urticariei idiopatice cronice la copii cu vârsta cuprinsă între 6 luni și 5 ani. Reduce semnificativ apariția, severitatea și durata urticariei și reduce semnificativ pruritul.
contraindicații
cetirizină clorhidrat soluție orală, USP este contraindicat la acei pacienți cu hipersensibilitate cunoscută la acesta sau la oricare dintre ingredientele sale sau la hidroxizină.
Precauții
activități care necesită vigilență mentală: în studiile clinice, a fost raportată apariția somnolenței la unii pacienți care au luat clorhidrat de cetirizină; prin urmare, trebuie să se acorde atenția cuvenită atunci când conduceți un vehicul sau folosiți utilaje potențial periculoase. Trebuie evitată utilizarea concomitentă a clorhidratului de cetirizină cu alcool etilic sau cu alte deprimante ale SNC, deoarece pot apărea reduceri suplimentare ale vigilenței și afectarea suplimentară a performanței SNC.interacțiuni medicamentoase: nu s-au găsit interacțiuni medicamentoase semnificative clinic cu teofilina în doză mică, azitromicină, pseudoefedrină, ketoconazol sau eritromicină. A existat o mică scădere a clearance-ului cetirizinei cauzată de o doză de teofilină de 400 mg; este posibil ca dozele mai mari de teofilină să aibă un efect mai mare.
carcinogeneză, mutageneză și afectarea fertilității: într-un studiu de carcinogenitate cu durata de 2 ani la șobolani, cetirizina nu a fost carcinogenă la doze dietetice de până la 20 mg/kg (de aproximativ 15 ori doza zilnică maximă recomandată pe cale orală la adulți, în mg/m2, sau de aproximativ 7 ori doza zilnică maximă recomandată pe cale orală la sugari, în mg / m2). Într-un studiu de carcinogenitate cu durata de 2 ani la șoarece, Cetirizina a determinat o incidență crescută a tumorilor hepatice benigne la bărbați la o doză alimentară de 16 mg/kg (de aproximativ 6 ori doza zilnică maximă recomandată pe cale orală la adulți în mg/m2 sau de aproximativ 3 ori doza zilnică maximă recomandată pe cale orală la sugari în mg/m2). Nu s-a observat o creștere a incidenței tumorilor hepatice la șoareci la o doză dietetică de 4 mg/kg (de aproximativ 2 ori doza zilnică maximă recomandată pe cale orală la adulți pe bază de mg/m2 sau aproximativ echivalentă cu doza zilnică maximă recomandată pe cale orală la sugari pe bază de mg/m2). Semnificația clinică a acestor constatări în timpul utilizării pe termen lung a clorhidratului de cetirizină nu este cunoscută.cetirizina nu a fost mutagenă în testul Ames și nu a fost clastogenă în testul limfocitelor umane, testul limfomului de șoarece și testul micronucleilor in vivo la șobolani.
într-un studiu privind fertilitatea și performanța reproductivă generală la șoareci, cetirizina nu a afectat fertilitatea la o doză orală de 64 mg/kg (de aproximativ 25 de ori mai mare decât doza zilnică maximă recomandată pe cale orală la adulți, în mg/m2).
utilizare pediatrică: siguranța clorhidratului de cetirizină a fost demonstrată la pacienții pediatrici cu vârsta cuprinsă între 6 și 5 ani. Siguranța cetirizinei a fost demonstrată la 168 de pacienți cu vârsta cuprinsă între 2 și 5 ani în studii controlate cu placebo, cu o durată de până la 4 săptămâni. Pe bază de mg/kg, majoritatea celor 168 de pacienți au primit între 0, 2 și 0, 4 mg / kg de cetirizină HCl. Siguranța cetirizinei la 399 de pacienți cu vârsta cuprinsă între 12 și 24 de luni a fost demonstrată într-un studiu controlat cu placebo cu durata de 18 luni, în care doza medie a fost
0,25 mg/kg de două ori pe zi, corespunzând unui interval cuprins între 4 și 11 mg/zi. Siguranța soluției orale de clorhidrat de cetirizină, USP, a fost demonstrată la 42 de pacienți cu vârsta cuprinsă între 6 și 11 luni într-un studiu controlat cu placebo de 7 zile. Doza prescrisă a fost de 0, 25 mg/kg de două ori pe zi, ceea ce a corespuns unei medii de 4, 5 mg/zi, cu un interval cuprins între 3, 4 și 6, 2 mg/zi.eficacitatea clorhidratului de cetirizină pentru tratamentul rinitei alergice și urticariei idiopatice cronice la copii și adolescenți cu vârsta cuprinsă între 6 și 5 ani se bazează pe o extrapolare a eficacității demonstrate a clorhidratului de cetirizină la adulții cu aceste afecțiuni și probabilitatea ca evoluția bolii, fiziopatologia și efectul medicamentului să fie substanțial similare între aceste două populații. Eficacitatea este extrapolată până la vârsta de 6 luni pentru rinita alergică perenă, deoarece se crede că această boală apare până la aceste vârste la copii. Dozele recomandate pentru populația pediatrică se bazează pe comparații încrucișate ale farmacocineticii și farmacodinamicii cetirizinei la subiecții adulți și pediatrici și pe profilul de siguranță al cetirizinei atât la pacienții adulți, cât și la copii și adolescenți, la doze egale sau mai mari decât dozele recomandate. Cetirizina ASC și C max la subiecții pediatrici cu vârsta cuprinsă între 6 și 23 de luni care au primit o medie de 2.3 mg într-o doză unică și la subiecții cu vârsta cuprinsă între 2 și 5 ani care au primit o doză unică de 5 mg soluție orală de cetirizină, s-a estimat a fi intermediar între cel observat la adulții care au primit o doză unică de 10 mg comprimate de cetirizină și cei care au primit o doză unică de 20 mg comprimate de cetirizină.
siguranța și eficacitatea cetirizinei la copii și adolescenți cu vârsta sub 6 luni nu au fost stabilite.
reacții Adverse
studiile pediatrice au fost efectuate cu clorhidrat de cetirizină. Peste 1300 de pacienți pediatrici cu vârsta cuprinsă între 6 și 11 ani, cu peste 900 tratați cu clorhidrat de cetirizină în doze de 1,25 până la 10 mg pe zi, au fost incluși în studiile clinice controlate și necontrolate efectuate în Statele Unite. Durata tratamentului a variat de la 2 la 12 săptămâni. Studiile controlate cu Placebo cu durata de până la 4 săptămâni au inclus 168 de pacienți pediatrici cu vârsta cuprinsă între 2 și 5 ani care au primit cetirizină, dintre care majoritatea au primit doze zilnice unice de 5 mg. Un studiu controlat cu placebo cu durata de 18 luni a inclus 399 de pacienți cu vârsta cuprinsă între 12 și 24 de luni tratați cu cetirizină (0.25 mg/kg de două ori pe zi) și un alt studiu controlat cu placebo, cu durata de 7 zile, a inclus 42 de pacienți cu vârsta cuprinsă între 6 și 11 luni care au fost tratați cu cetirizină (0, 25 mg/kg de două ori pe zi).
majoritatea reacțiilor adverse raportate la copii și adolescenți cu vârsta cuprinsă între 2 și 11 ani cu clorhidrat de cetirizină au fost ușoare sau moderate. În studiile controlate cu placebo, incidența întreruperilor datorate reacțiilor adverse la copii și adolescenți cărora li s-a administrat până la 10 mg clorhidrat de cetirizină a fost mai puțin frecventă (0,4% pentru clorhidrat de cetirizină față de 1,0% pentru placebo).
Tabelul 1 enumeră reacțiile adverse care au fost raportate pentru clorhidratul de cetirizină 5 și 10 mg la copii și adolescenți cu vârsta cuprinsă între 6 și 11 ani în studiile clinice controlate cu placebo din Statele Unite și au fost mai frecvente cu clorhidratul de cetirizină decât placebo. Dintre acestea, durerea abdominală a fost considerată legată de tratament, iar somnolența pare să fie dependentă de doză, 1,3% în cazul placebo, 1,9% în cazul administrării de 5 mg și 4,2% în cazul administrării de 10 mg. Reacțiile adverse raportate la copii și adolescenți cu vârsta cuprinsă între 2 și 5 ani în studiile controlate cu placebo au fost de natură similară din punct de vedere calitativ și, în general, similare ca frecvență cu cele raportate în studiile la copii cu vârsta cuprinsă între 6 și 11 ani.
în studiile controlate cu placebo la copii și adolescenți cu vârsta cuprinsă între 6 și 24 de luni, incidența reacțiilor adverse a fost similară în grupurile de tratament cu cetirizină și placebo din fiecare studiu. Somnolența a apărut cu aproximativ aceeași frecvență la pacienții cărora li s-a administrat cetirizină și la pacienții cărora li s-a administrat placebo. Într-un studiu cu durata de 1 săptămână la copii cu vârsta cuprinsă între 6 și 11 luni, pacienții cărora li s-a administrat cetirizină au prezentat o iritabilitate/stare de nervozitate mai mare decât pacienții cărora li s-a administrat placebo. Într-un studiu cu durata de 18 luni la pacienți cu vârsta de 12 luni și peste, insomnia a apărut mai frecvent la pacienții cărora li s-a administrat cetirizină comparativ cu pacienții cărora li s-a administrat placebo (9,0% față de 5,3%). La pacienții cărora li s-a administrat cetirizină 5 mg sau mai mult pe zi, comparativ cu pacienții cărora li s-a administrat placebo, oboseala (3,6% față de 1,3%) și starea generală de rău (3,6% față de 1,8%) au apărut mai frecvent.
Tabelul 1.
Adverse Experiences Reported in Pediatric Patients Aged 6 to 11 Years in Placebo-Controlled United States Cetirizine Hydrochloride Trials (5 or 10 mg Dose) Which Occurred at a Frequency of >2% in Either the 5 mg or the 10 mg Cetirizine Hydrochloride Group, and More Frequently Than in the Placebo Group
| Adverse Experiences | Placebo (N=309) |
Cetirizine Hydrochloride | |
| 5 mg (N=161) |
10mg (N=215) |
||
| Headache | 12.3% | 11.0% | 14.0% |
| Pharyngitis | 2.9% | 6.2% | 2.8% |
| Abdominal Pains | 1.9% | 4.4% | 5.6% |
| Coughing | 3.9% | 4.4% | 2.8% |
| Somnolence | 1.3% | 1.9% | 4.2% |
| Diarrhea | 1.3% | 3.1% | 1.9% |
| Epistaxis | 2.9% | 3.7% | 1.9% |
| bronhospasm | 1, 9% | 3, 1% | 1, 9% | greață | 1, 9% | 1, 9% | 2, 8% | vărsături | 1,0% | 2,5% | 2,3% |
următoarele evenimente au fost observate rar (mai puțin de 2%), fie la 3982 adulți și copii cu vârsta de 12 ani și peste sau la 659 de pacienți pediatrici cu vârsta cuprinsă între 6 și 11 ani care au primit clorhidrat de cetirizină în studiile din SUA, inclusiv un studiu deschis pentru adulți cu o durată de șase luni. Nu a fost stabilită o relație cauzală a acestor evenimente rare cu administrarea clorhidratului de cetirizină.
sistemul nervos autonom: anorexie, înroșirea feței, salivație crescută, retenție urinară.
cardiovasculare: insuficiență cardiacă, hipertensiune arterială, palpitații, tahicardie.
sisteme nervoase centrale și periferice: coordonare anormală, ataxie, confuzie, disfonie, hiperestezie, hiperkinezie, hipertonie, hipoestezie, crampe la nivelul picioarelor, migrenă, mielită, paralizie, parestezie, ptoză, sincopă, tremor, spasme, vertij, defect de câmp vizual.
gastro-intestinale: funcție hepatică anormală, carii dentare agravate, constipație, dispepsie, eructație, flatulență, gastrită, hemoroizi, apetit crescut, melenă, hemoragie rectală, stomatită, inclusiv stomatită ulcerativă, decolorarea limbii, edem al limbii.
genito-urinar: cistită, disurie, hematurie, frecvență de micțiune, poliurie, incontinență urinară, infecții ale tractului urinar.
auz și Vestibular: surditate, durere de urechi, ototoxicitate, tinitus.
Metabolic / nutrițional: deshidratare, diabet zaharat, sete.
musculo-scheletice: artralgie, artrită, artroză, slăbiciune musculară, mialgie.
psihiatric: gândire anormală, agitație, amnezie, anxietate, scăderea libidoului, depersonalizare, depresie, labilitate emoțională, euforie, concentrare afectată, insomnie, nervozitate, paronirie, tulburări de somn.
sistemul respirator: bronșită, dispnee, hiperventilație, spută crescută, pneumonie, tulburări respiratorii, rinită, sinuzită, infecții ale tractului respirator superior.
reproductivă: dismenoree, dureri de sân la femei, sângerări intermenstruale, leucoree, menoragie, vaginită.
reticuloendotelial: limfadenopatie.
piele: acnee, alopecie, angioedem, erupție buloasă, dermatită, piele uscată, eczemă, erupție eritematoasă, furunculoză, hiperkeratoză, hipertricoză, transpirație crescută, erupție maculopapulară, reacție de fotosensibilitate, reacție toxică de fotosensibilitate, prurit, purpură, erupție cutanată, seboree, afecțiuni cutanate, nodul cutanat, urticarie.
simțuri speciale: parosmie, pierderea gustului, pervertirea gustului.
viziune: orbire, conjunctivită, dureri oculare, glaucom, pierderea cazării, hemoragie oculară, xeroftalmie.
corpul ca întreg: leziuni accidentale, astenie, dureri de spate, dureri toracice, abdomen mărit, edem facial, febră, edem generalizat, bufeuri, greutate crescută, edem picior, stare generală de rău, polip nazal, durere, paloare, edem periorbital, edem periferic, rigori.în timpul tratamentului cu cetirizină au apărut cazuri ocazionale de creșteri tranzitorii, reversibile ale transaminazelor hepatice. A fost raportată hepatită cu creștere semnificativă a transaminazelor și bilirubină crescută în asociere cu utilizarea clorhidratului de cetirizină.
experiența după punerea pe piață
în perioada de după punerea pe piață, au fost raportate următoarele evenimente adverse rare, dar potențial severe: reacție agresivă, anafilaxie, colestază, convulsii, glomerulonefrită, halucinații, anemie hemolitică, hepatită, dischinezie orofacială, hipotensiune arterială severă, naștere mortală, ideație suicidară, suicid, trombocitopenie și pustuloză exantematoasă acută generalizată (AGEP).
pentru a raporta reacțiile adverse suspectate, contactați Torrent Pharma Inc. la 800-912-9561 sau FDA la 1-800-FDA – 1088 sau www.fda.gov/medwatch.
abuzul și dependența de droguri
nu există informații care să indice că abuzul sau dependența apare cu clorhidratul de cetirizină.
supradozajul
a fost raportat supradozajul cu clorhidrat de cetirizină. La un pacient adult care a luat 150 mg clorhidrat de cetirizină, pacientul a fost somnolent, dar nu a prezentat alte semne clinice sau rezultate anormale ale chimiei sângelui sau ale hematologiei. La un pacient pediatru în vârstă de 18 luni care a luat o supradoză de clorhidrat de cetirizină (aproximativ 180 mg), au fost observate inițial neliniște și iritabilitate; aceasta a fost urmată de somnolență. În caz de supradozaj, tratamentul trebuie să fie simptomatic sau de susținere, luând în considerare orice medicamente ingerate concomitent. Nu se cunoaște un antidot specific pentru clorhidratul de cetirizină. Clorhidratul de cetirizină nu este eliminat eficient prin dializă, iar dializa va fi ineficientă decât dacă un agent dializabil a fost ingerat concomitent. Dozele orale letale minime acute au fost de 237 mg/kg la șoarece (de aproximativ 95 de ori doza orală zilnică maximă recomandată la adulți, în mg/m2, sau de aproximativ 40 de ori doza orală zilnică maximă recomandată la sugari, în mg/m2) și de 562 mg/kg la șobolan (de aproximativ 460 de ori doza orală zilnică maximă recomandată la adulți, în mg/m2, sau de aproximativ 190 de ori doza orală zilnică maximă recomandată la sugari, în mg / m2. La rozătoare, ținta toxicității acute a fost sistemul nervos central, iar ținta toxicității după doze multiple a fost ficatul.
dozare& administrare
soluție orală de clorhidrat de cetirizină, USP poate fi luată fără a ține cont de consumul alimentar.
copii cu vârsta cuprinsă între 2 și 5 ani pentru urticarie cronică: doza inițială recomandată de soluție orală de clorhidrat de cetirizină, USP la copiii cu vârsta cuprinsă între 2 și 5 ani este de 2,5 mg (o linguriță de o mie) soluție orală o dată pe zi. Doza la această grupă de vârstă poate fi crescută la o doză maximă de 5 mg pe zi administrată sub formă de 1 linguriță soluție orală o dată pe zi sau o linguriță de soluție orală la fiecare 12 ore.
copii cu vârsta cuprinsă între 6 luni și< 2 ani pentru rinita alergică perenă și Urticaria cronică: doza recomandată de soluție orală de clorhidrat de cetirizină, USP la copii cu vârsta cuprinsă între 6 luni și 23 luni este de 2,5 mg (o linguriță de o mie) o dată pe zi. Doza la copiii cu vârsta cuprinsă între 12 și 23 de luni poate fi crescută la o doză maximă de 5 mg pe zi, administrată sub formă de linguriță de 2,5 mg la fiecare 12 ore.
cum se furnizează cetirizină
soluție orală de clorhidrat de cetirizină, USP 5 mg/5 mL (1 mg / mL) este o soluție orală incoloră până la ușor gălbuie, furnizată în flacoane de 120 mL.flacoane de 120 mL NDC 13668-029-07
soluție orală de clorhidrat de cetirizină, USP 5 mg/5 mL (1 mg / mL) este o soluție orală incoloră până la ușor gălbuie, furnizată în flacoane de 480 mL.
de Sticle de 480 mL NDC 13668-029-11
STOCARE
Magazin la 20°-25°C (68°-77°F); excursii permise la 15°-30°C (59°-86°F) .
numai Rx
fabricat de:
Bio-Pharm, Inc.Levittown, PA 19057
fabricat pentru:
TORRENT PHARMA INC.
150 Allen Road, Suite 102
Basking Ridge, NJ 07920
PRINCIPAL DISPLAY PANEL – Bottle Label
NDC 13668-029-07
Cetirizine Hydrochloride Oral Solution, USP
1 mg/mL
FOR ORAL USE ONLY
120 mL
Rx only

NDC 13668-029-11
Cetirizine Hydrochloride Oral Solution, USP
1 mg/mL
FOR ORAL USE ONLY
480 mL
Rx only

| Cetirizine HYDROCHLORIDE ORAL SOLUTION Cetirizine hydrochloride oral solution solution |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Labeler – Torrent Pharma, Inc. (916488547)
Registrant – Torrent Pharma Inc (790033935)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Torrent Pharmaceuticals Limited | 916488547 | manufacture(13668-029), analysis(13668-029), pack(13668-029), label(13668-029) | |
Frequently asked questions
- Should cetirizine be taken at bedtime or upon awakening? Și înainte sau după o anumită masă?
mai multe despre cetirizină
- efecte secundare
- în timpul sarcinii sau alăptării
- informații privind dozajul
- Sfaturi pentru pacienți
- imagini medicamentoase
- interacțiuni medicamentoase
- comparați alternativele
- grup de sprijin
- prețuri& cupoane
- 225 comentarii
- clasa de droguri: antihistamines
Consumer resources
- Patient Information
- Cetirizine Intravenous (Advanced Reading)
Professional resources
- Prescribing Information
- Cetirizine (Systemic) (Professional Patient Advice)
- Cetirizine Oral Solution (FDA)
- Cetirizine Tablets (FDA)
- Cetirizine Tablets Chewable (FDA)
Other brands Zyrtec, Aller-Tec, Quzyttir, All Day Allergy, … + 3 mai
ghiduri de tratament înrudite
- rinită alergică
- urticarie
- disfuncția tubului Eustachian
- urticarie fizică
Disclaimer Medical
Leave a Reply